3D荧光断层扫描技术在CAR-T方向的应用
作为设备销售商,我们总是期望新的设计和技术可以应用于一些热点研究方向,那么新型的三维荧光断层扫描成像技术(Insyte FLECT/CT:http://www.trifoilimaging.com)是否可以应用于CAR-T研究呢?
直接而简短的回答:是的,可以!
CAR-T细胞(嵌合抗原受体)疗法是一种癌症治疗策略,通过收集患者自身的T细胞,一种攻击患病细胞(如癌细胞)的免疫细胞,然后利用基因工程技术使其能够识别在癌细胞上表达的抗原。这些经过改造后的特异性免疫细胞被称为CAR-T细胞,当它们被重新注入病人体内后,来自病人自身的、已经过改造的CAR-T细胞便可以攻击并杀死癌细胞。在实际应用时,CAR-T细胞往往需要一种特殊蛋白质(细胞因子)的局部激活来刺激其产生杀伤功能。这也使得常规的ACT(Adoptive cell therapy)疗法虽然对白血病等疾病有效,但很少能成功治疗实体肿瘤。
我们选择了最近发表于Science Advances期刊上的一项研究成果(doi: 10.1126/sciadv.abn8264),以它为例说明Insyte FLECT/CT技术在此研究方向的应用价值。
斯坦福大学研究团队研发了一种增强CAR-T细胞对实体肿瘤杀伤力的递送方法。研究人员使用了一种基于水凝胶的传递系统,将CAR-T细胞和用于激活其杀伤功能的细胞因子共同添加到水凝胶中,然后将混合物注射到肿瘤附近。一旦CAR-T细胞到达病灶区域,细胞因子将直接刺激CAR-T细胞产生杀伤活性。
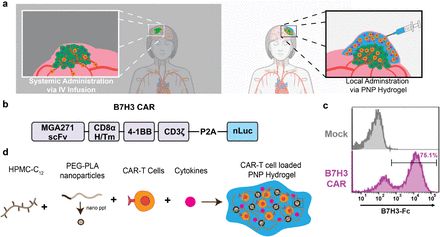
本次研究中,研究人员使用基于生物发光的in vivo光学成像技术,对以下3个方面的实验结果进行监测:
1、观察基于水凝胶的给药系统在小鼠体内随时间的稳定性/降解情况。研究人员使用了一种近红外荧光团(Alexa Fuor 647)与混合在水凝胶中的纳米颗粒结合,然后将这些水凝胶植入小鼠体内,并在设定时间内进行成像。
2、跟踪注射后的CAR-T细胞:CAR-T细胞经过基因修饰后,不仅可以识别特定的肿瘤抗原,而且可以表达荧光素酶(LUC),用于生物发光成像。
3、评估CAR-T治疗效果:经过修饰后的癌细胞(MED8A, human medulloblastoma brain cancer)也可表达LUC,用于生物发光成像。将这些癌细胞注射到小鼠皮下,建立皮下肿瘤模型。在注射CAR-T细胞进行治疗后,可以观察到来自肿瘤的生物发光信号,并且信号强度随时间的推移而下降,表明该种CAR-T给药系统对于实体肿瘤有明显的治疗效果。
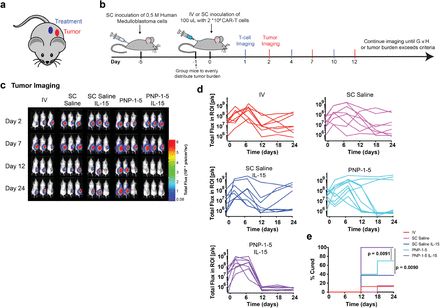
如果在上述研究中使用3D荧光断层扫描成像来替代生物发光成像,会对实验过程及结果有哪些提高呢?
首先,研究人员可以使用近红外荧光蛋白(iRFP)来替代LUC对肿瘤细胞进行标记,这种方法的优点是在后续成像时不再需要额外注入底物(荧光素)用于生物发光成像。由于影响生物发光过程的因素很多,包括底物浓度、氧气、ATP、肿瘤大小、温度等,从而间接影响对递送系统疗效的评估。而利用iRFP进行荧光成像时,由于信号采集完全依靠激发光/发射光,不受其它因素的干扰,可有效避免荧光素底物可能对实验结果产生的影响,得到更加稳定的定量结果,从而能够更加准确地评估CAR-T递送系统的治疗效果。
其次,研究人员可以把皮下肿瘤设计为原位肿瘤。尽管这项研究的主要目的在于评估基于水凝胶的CAR-T给药系统的疗效,但如果能够在此基础上引入InSyTe FLECT/CT,便可以更进一步地实现对于CAR-T在原位(即深层组织模型)中的疗效监测。毫无疑问,3D荧光断层扫描技术的应用,能够协助研究人员获得更多更全面的实验数据,这些数据也将更加有助于对实验结果的评估,在实验结果向临床转化的过程中发挥出巨大的价值。
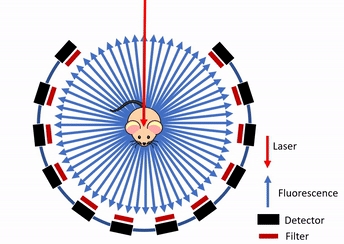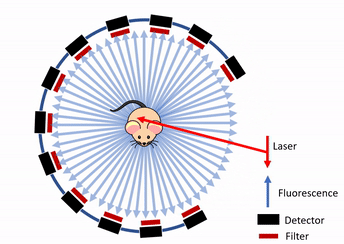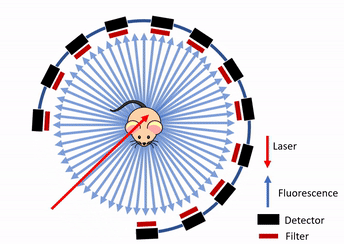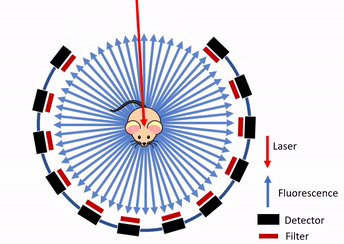
本文仅以原文献中的成像方法为例进行技术讨论,不对原文实验结果有任何评价性的结论。
技术服务联系方式:
孙元元(技术部)
Tel:13810818543
柴丹(销售部)
Tel:13810910943
田建华(应用工程师)
Tel:18302907782
张婷瑞(应用工程师)
Tel:13910490151
联系邮箱:sales@bio-one.cn
联系电话:010-64841721/1727,64842355/2356,58294864/4669,13810818543
E-mail:13810818543@139.com





