慢性牙周炎患者龈沟液的微生物和代谢组学分析

文章标题:Microbial and metabolomics analysis of gingival crevicular fluid in general chronic periodontitis patients: lessons for a predictive, preventive, and personalized medical approach
发表期刊:EPMA Journal
发表时间:2020年4月
影响因子:6.543
合作客户:上海交通大学医学院口腔学院上海市第九人民医院
研究背景
慢性牙周炎(GCP)是一种细菌性炎症性疾病,由龈下多菌生物膜引起并维持;微生物群落与宿主的复杂相互作用破坏了宿主的体内平衡,破坏了组织附着,破坏了牙齿的支持结构。尽管发表了大量关于GCP患者口腔微生物群和代谢特征变化的研究,但缺乏关于宿主细菌相互作用和生化代谢之间相关性的信息。在本文中分析了口腔微生物组、口腔代谢组以及它们之间的联系,并确定潜在分子作为GCP中预测性、预防性和个性化药物(PPPM)的生物标记物。
研究结果
1.GCF牙周微生物群落结构的变化
为了描述牙周病患者口腔微生物群落与健康人口腔微生物群落的差异,分析了微生物群落的α和β多样性,以评估其总体组成丰富度和结构特征。α多样性指数包括Chao1指数、ACE指数、Shannon指数和Simpson指数,两组之间没有显著差异。然而,根据非度量多维尺度分析NMDS和基于OTU水平上未加权和加权UniFrac距离的β多样性分析表明,两组之间的差异具有统计学意义(P<0.01),表明总体微生物群落结构不同。结果表明,健康对照组和牙周炎患者之间的GCF微生物群落结构发生了显著变化。
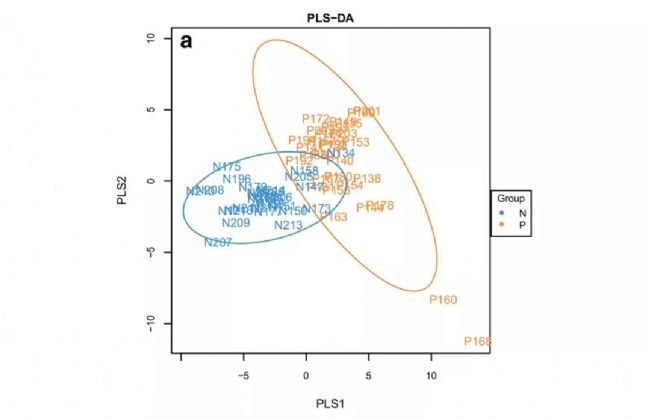

从总体GCF样本来看,优势门包括变形菌、厚壁菌、拟杆菌、放线菌、梭杆菌、螺旋体和协同菌(>总丰度的99%)。其中最丰富的22个属,占总丰度的74.5%。在不同分类水平上用GraPhlAn构建的系统发育树,它可以快速识别从门到属的优势微生物类群。当分别分析两组样本时,牙周炎样本和健康样本之间优势类群的精确比例有所不同。
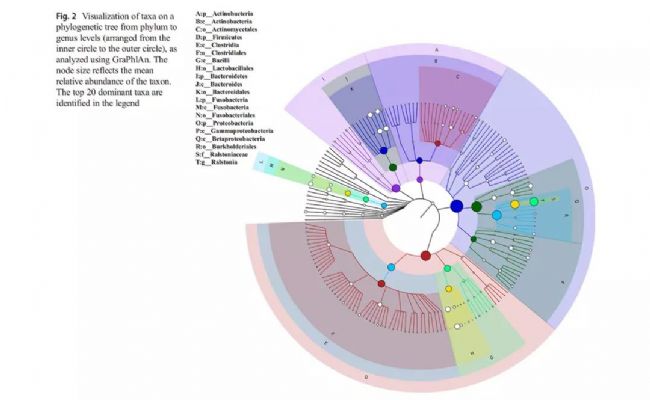
图2.从门到属的系统发育树上分类群的可视化
3. 牙周微生物群的功能变异
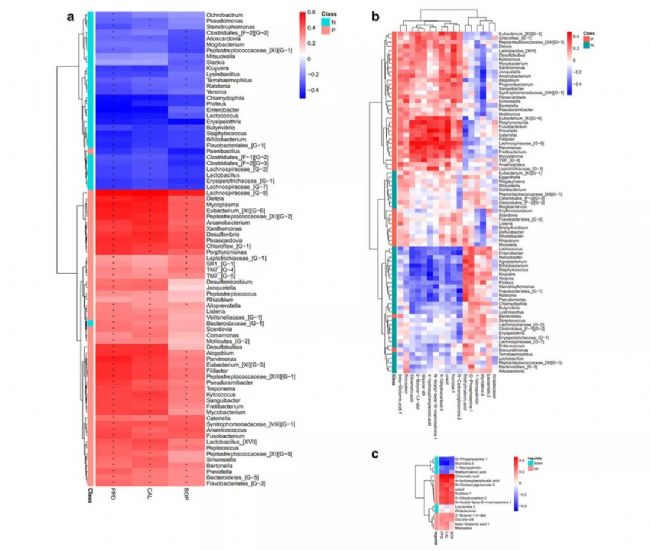
在门水平上,GCP患者的氯曲菌、协同菌、柔嫩菌、拟杆菌和梭杆菌的相对丰度显著高于健康对照组。然而,与牙周病患者相比,健康对照组中厚壁菌和衣原体的丰度相对较高。在属水平上,两个类群之间差异最大的前20个分类群。与健康对照组相比,牙周病患者中的隐球菌、类杆菌、迪茨氏菌、氯曲菌[G-1]、分枝杆菌、移动菌、支原体、副卡多夫菌、消化链球菌科[XIII][G-1]和真菌显著富集。相比之下,牙周病患者中的几个属,即变形杆菌、乳酸菌科菌[G-7]、乳酸杆菌、乳球菌、双歧杆菌、梭状芽孢杆菌[F-1][G-2]、肠杆菌、丹毒蓟马菌、丹毒霉科菌[G-1]和杆菌[G-1]的比例低于对照组。这些数据共同揭示了微生物在牙周病患者的GCF微生物组中的变化,表明存在微生物失调状态,以及预测了代谢功能的紊乱。
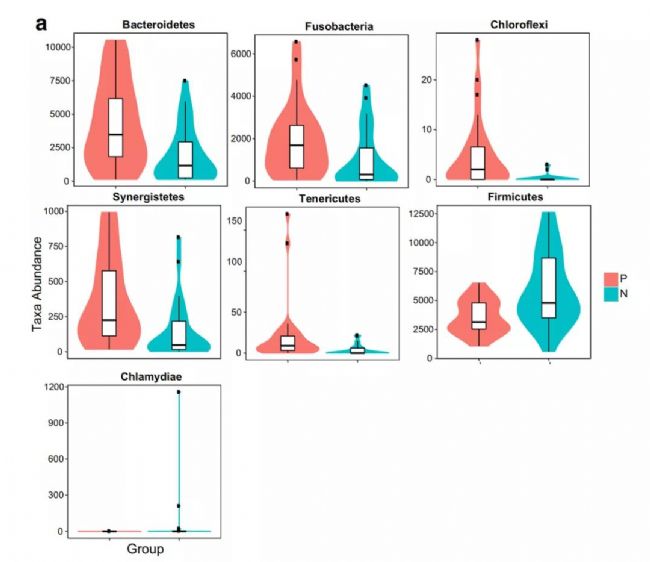
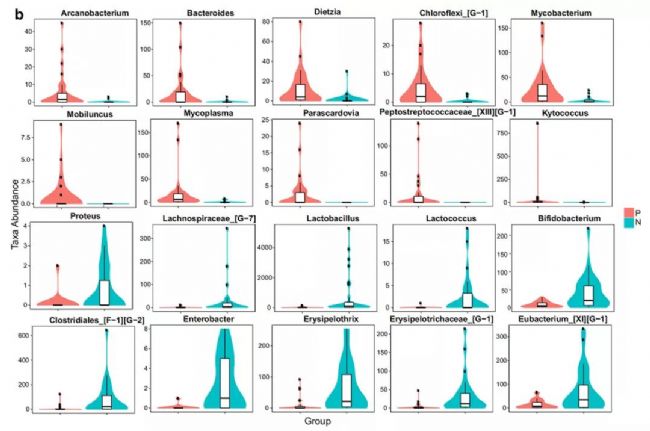
图3. 通过Metastats对GCP患者(P组)和健康对照组(N组)在门(a)和属(b)水平上的分类单元丰度进行统计比较
4.GCF样本代谢组学特征的变化
去除内标物和假阳性峰,合并同一代谢物的峰后,共获得147个定性代谢物。与对照组相比,牙周病患者表现出明显的代谢改变。与健康对照组相比,牙周病患者的GCF代谢物差异最大。为了进一步表征代谢物的特征,我们进行了代谢物集富集分析(MSEA)和拓扑分析,在牙周病组中,嘧啶代谢、D-谷氨酰胺和d-谷氨酰胺代谢被确定为显著过度表达的途径(分别为p=0.000488027和0.031594),这可能反映了疾病相关社区的代谢特征。
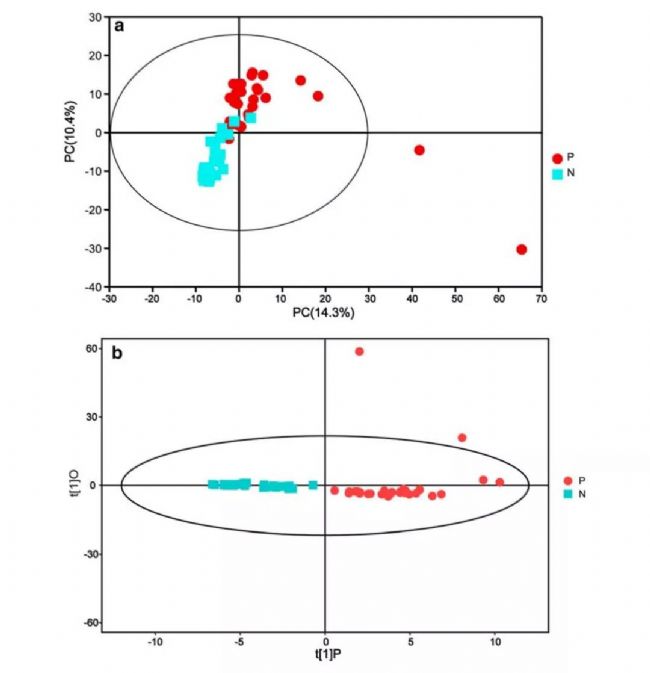
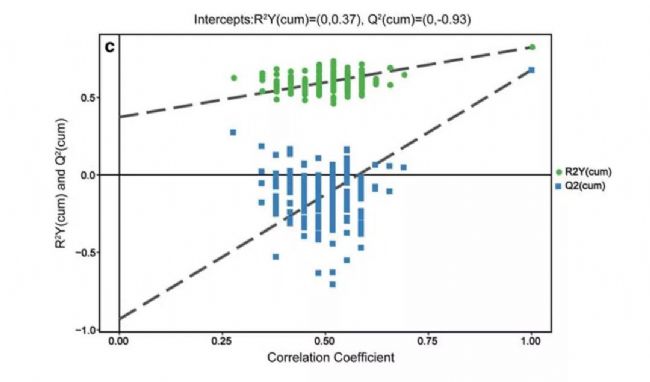
图4. 典型的气相色谱-质谱计分图
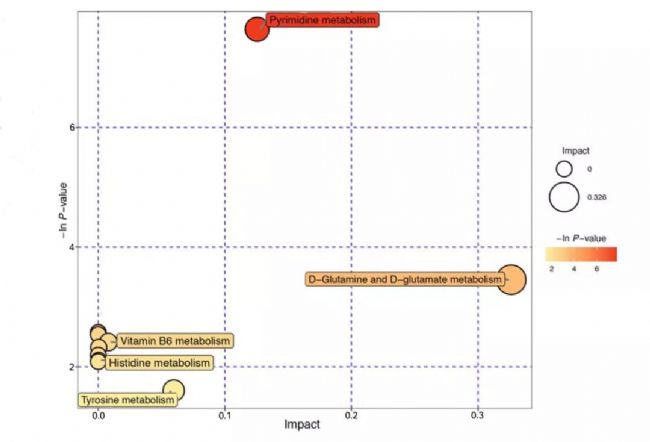
图5.代谢物集富集分析(MSEA)的气泡图和差异代谢物的拓扑分析
5.微生物群、代谢物和牙周临床指标之间的相关性
在口腔中检测到的细菌属与牙周炎的临床数据之间存在着很强的统计显著相关性。牙周病患者富集属与临床检测数据呈正相关,而健康对照富集属与临床数据呈负相关。值得注意的是,牙周病患者的大多数代谢物水平升高,并与大多数牙周病富集属呈正相关,与大多数健康对照富集属呈负相关。相反,牙周病个体中缺失的代谢产物水平,与许多健康对照丰富的属呈正相关,与牙周病丰富的属呈负相关。牙周病患者体内水平也降低的代谢物,与大多数牙周病富集的属有负相关和显著差异。具体而言,假定的牙周病细菌的属,如卟啉单胞菌、普氏菌、梭杆菌和产线菌,与差异代谢物密切相关。综上所述,口腔微生物群的改变在一定程度上与龈下代谢有关,GCF代谢物的水平可能反映了这些细菌种类丰度的变化。
牙周炎患者代谢物水平的升高与牙周炎的临床数据呈正相关,而代谢物水平的降低与临床数据呈负相关。也就是说,代谢产物水平的增加或减少变化越大,牙周炎的临床数据越大,临床特征越明显。这一结果增强了牙周炎临床条件下代谢物的变化。代谢物对BOP、CAL和PD的预测具有显著的积极作用,表明它们可能作为牙周炎症严重程度的指标。ROC曲线还表明,柠檬酸和N-氨甲酰谷氨酸联合应用对中度或重度牙周炎的诊断具有令人满意的准确性(AUC=0.876),这可能是牙周炎GCF中的有效生物标记物。总之,这些结果提供了对牙周益生菌群落代谢特征的洞察,并确定了炎症状态的潜在生物标志物。

文献原文下载链接:
https://pan.baidu.com/s/1kF0ChMpbp4OGz302AlhRyg
提取码:4nlw





