DNA羟甲基化和TET酶在胎盘发育和妊娠结局中的作用
大家好,这里是专注表观组学十余年,领跑多组学科研服务的易基因。
胎盘是支持哺乳动物胚胎和胎儿发育所必需的临时器官。了解滋养层细胞分化和胎盘功能的分子机制可能有助于改善产科并发症的诊断和治疗。印迹基因是调控胎盘发育的基础,表观遗传学在基因表达(尤其是印迹基因)的调控中起着重要作用。TET酶(Ten-Eleven-Translocation enzymes)是表观遗传学机制的一部分,可以将5-甲基胞嘧啶(5mC)转化为5-羟甲基胞嘧啶(5hmC)。
DNA羟甲基化是DNA去甲基化机制中的中间体,并可能是一种稳定且功能相关的表观遗传学标记。DNA羟甲基化在胎盘分化和发育过程中的作用尚不完全清楚,但该领域知识的增加将有助于评估其在妊娠并发症中的潜在作用。本文综述了DNA羟甲基化及其表观遗传调控因子在人和小鼠胎盘发育和功能中的作用,并在基因组印迹机制和妊娠并发症(如宫内生长受限,先兆子痫和妊娠丢失)的背景下对5hmC进行探讨。累积的研究结果表明,DNA羟甲基化可能对调控胎盘中的基因表达非常重要,并提示在妊娠期间滋养层细胞分化中起着动态作用。
胎盘是由具有特殊功能的不同细胞类型组成的高度组织化器官,小鼠和人的胎盘发育在结构和分子水平上存在显著差异。在人胎盘发育过程中,单核细胞滋养层(cytotrophoblas,CTB)细胞向蜕膜间隙的迁移标志着初级胎盘绒毛形成的开始。这些CTB分化为绒毛外CTB,具有侵袭性并参与植入过程。此外,这些CTB还分化为绒毛CTB,融合并随后形成合胞体滋养层(syncytiotrophoblast,STB)细胞,在绒毛树表面形成连续的合胞体层,并与流经绒毛间隙的母体血液直接接触,从而实现母体-胎儿交换。在整个妊娠过程中,STB细胞通过持续融合初级CTB细胞来维持,因此在STB细胞内可以观察到不同程度染色质浓缩的细胞核形态。虽然大多数细胞核分散在合胞体内,但其他细胞核聚集在末端绒毛表面(合胞结)。因此,绒毛结构由包含胎儿血管的间充质核心、CTB层和STB外层组成(图1)。
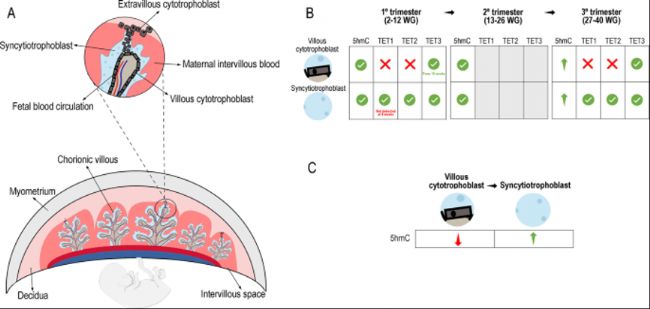
绿色√标记:存在5hmC或表观遗传调控因子表达;红色X标记:不存在5hmC或表观遗传调控因子表达;绿色箭头⬆:5hmC或表观遗传调控因子水平增加;红色箭头⬇:5hmC或表观遗传调控因子水平降低;灰色方块:未研究
在小鼠中,胎儿-母体交换发生在与人绒毛胎盘类似的“迷宫(labyrinth)”中,其具有复杂的母体和胎儿血管通道序列。“迷宫”上方有一个由具有内分泌功能的滋养层巨细胞(trophoblast giant cell,TGC)、海绵滋养层细胞(spongiotrophoblast,SpT)和糖原滋养层细胞(glycogen trophoblast cell,GlyT)组成的结合区域(图2)。
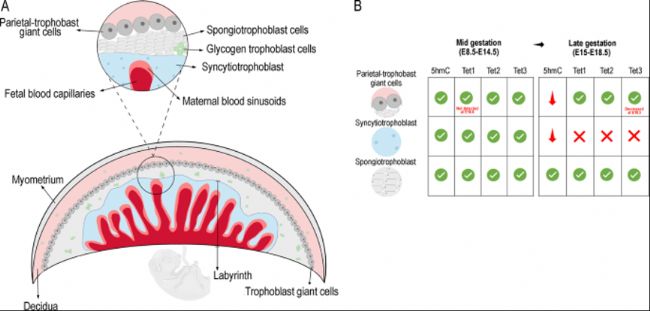
图2:小鼠胎盘
胎盘发育中的TET酶与DNA羟甲基化
TET酶参与胎盘滋养层细胞的分化和调控,5hmC水平失调导致胎盘异常发育。目前关于TET酶和DNA羟甲基化在胎盘发育中的作用研究有限。先前研究表明,胎盘基因组中的5hmC水平显著低于5mC水平。然而在以下两项研究中鉴定了CpG位点的存在,其5hmC水平持续增加,高于特定阈值且在样品之间可重复。Green等团队研究揭示了约21000个位点的5hmC平均值为13.73%,Mora等团队检测到约17000个CpG位点的5hmC富集。两项研究均揭示了5hmC在公海(基因组中分离的CpG)和大陆架(距离CpG岛2-4 kb)区域富集,而在CpG岛中缺失。另外还检测到5hmC在基因体、5’ UTR和3’UTR区域中富集,在近端启动子(距TSS约 200–1500 bp)和TSS区域缺失。Green等报告了稳定增强子中的富集和活性增强子内的缺失,而Mora等报告印迹基因(如GNAS和H19)和胎盘特异性DMR中的5hmC,通常与亲本等位基因5mC相关区域重叠。Green等研究表明,与活跃转录基因相比,转录失活基因中的5mC和5hmC水平均增加,其中5hmC与转录呈正相关。明显矛盾的研究结果可能归因于周转率的增加,周转率增加与在转录失活基因中观察到的甲基化水平增加有关,这些基因转化为羟甲基化水平增加。5hmC也更可能发生在妊娠中期和足月胎盘之间的差异表达基因中。
在人胎盘中,Fogarty等团队研究表明,与CTB细胞相比,5hmC在STB中更为富集,其中20–50%的STB细胞核在妊娠早期和中期呈阳性(positive),50%的STB细胞核在妊娠晚期呈阳性,尤其是在完全由5hmC阳性细胞核组成的合胞结中。相比之下,大多数STB细胞核在妊娠期间的5mC染色水平不显著,而超50%的CTB细胞核为5mC阳性(28)。Wilson等团队使用免疫荧光法分析结果表明,与妊娠早期和中期胎盘相比,足月胎盘的CTB和STB细胞中5hmC(和5mC)均增加(图1B)。在妊娠早期和中期,STB细胞中的5hmC染色更为显著(图1C)。在整个妊娠期间,随着CTB融合产生STB,STB中可能沉积5hmC,尤其在合胞结中,可能表明结形成过程中发生的氧化损伤。这些结果表明两种细胞类型之间的差异可能揭示其不同功能。例如绒毛滋养层细胞调节气体和营养交换,而STB在整个妊娠期间产生和分泌大量激素,揭示了该组织的高转录和翻译能力。如Rouault等团队研究结果揭示了CTB和STB的特异性转录组谱。
在小鼠胎盘中,在胚胎期(E)第8.5天,小鼠胎盘外胎盘锥体细胞(ectoplacental cone cell,EPC)和顶叶TGC(parietal-TGC)表现出5hmC高水平和5mC低水平。E10.5-E18.5期间所有“迷宫”细胞中维持细胞核内5mC水平,STB细胞核在整个妊娠期间呈现出5mC高水平。在E10.5时,所有“迷宫”滋养层细胞中均表现出5hmC高水平,但E18.5时水平逐渐降低。顶叶TGC在5hmC中逐渐降低,但5mC水平在E18.5时稳定增加(图2B)。总之,这些研究强调了不同滋养层细胞来源细胞类型的表观基因组动态变化,且在妊娠期间发生变化。
另一方面,关于TET酶在滋养层细胞分化过程中的作用研究较少。TET酶的敲低模型表明,5hmC对于维持发育和早期胚胎发生至关重要。Yamaguchi等团队研究表明,与对照组相比,父系TET1-KO小鼠可导致包括胎盘缺陷在内的多种表型,父系TET1-KO小鼠的胎盘显著缩小。Rakoczy等团队研究了TET酶在小鼠和人胎盘中的表达,小鼠中Tet1、Tet2和Tet3 mRNA在E8.5的绒毛膜、EPC和卵黄囊中表达,在E10.5~E12.5的“迷宫”(包括窦性TGC和STB细胞)中表达。而Tet1-3只在E14.5~E18.5的窦性TGC中表达,在STB中Tet不表达,这与妊娠晚期STB中观察到的5hmC水平一致。对于SpT细胞,Tet1-3在整个妊娠期间持续表达,而在GlyT细胞中仅在E14.5-E16.5之间显著强表达。除E10.5和E18.5分别出现Tet1表达缺失和Tet3表达降低外,顶叶TGC在整个妊娠期间的所有TET中均表达(图2B)。因此在E18.5时,顶叶TGC中5hmC水平降低与Tet3表达下调结果一致。在人胎盘的妊娠早期和晚期的STB细胞中检测到TET1-3蛋白,但在妊娠8周(weeks of gestation,WG)时除外(TET1未检测到)。绒毛CTB细胞在妊娠早期和晚期TET1和TET2不表达,TET3从10WG~足月期间均表达(图1B)。这些研究结果表明TET1和TET2在STB分化中起着重要作用。与CTB仅TET3表达相比,STB中5hmC的较高水平可能是三种TET在STB均表达的结果。由于胎盘发育是一个高度动态的过程,因此研究这些酶在妊娠中期胎盘中的表达也很重要。
关于TET酶的非催化作用,TET酶与一些表观遗传修饰因子(如组蛋白修饰酶)相互作用,导致TET靶向基因的抑制。如有研究表明TET1和EZH2之间的相互作用,它负责调控H3K27me3(一种在CTB细胞核中的组蛋白标记)和其他组蛋白修饰。
虽然胎盘结构在不同细胞类型中存在差异,但在妊娠期间的人和小鼠滋养层细胞中观察到5mC和5hmC以及TET表达。在妊娠末期可能会出现STB异常,因为在小鼠中TET不表达,但在人胎盘中TET表达。整个妊娠期间,在人类中5hmC水平增加,而在小鼠中5hmC降低。当然,还需要更多的研究来证实小鼠和人类之间的差异,并阐明其在胎盘发育过程中在细胞调控和分化中的作用。
胎盘印记基因中的DNA羟甲基化
1984年的细胞核移植实验首次描述了基因组印迹,带有两组母系染色体(雌核发育(gynogenotes))或两组父系染色体(雄核发育(androgenote))的小鼠胚胎无法正常发育,前者表现为胚胎外组织(胎盘和卵黄囊)生长迟缓和异常发育,后者表现为胚胎外组织过度生长和胚胎本身发育不良。实验结果表明尽管遗传信息相似,但遗传的母系和父系染色体在功能上并不相同。基因组印迹是一种表观遗传机制,其中印迹基因表现为单等位基因和亲本依赖性表达,受DNA差异甲基化区域(DMR)调控。其中一些DMR充当印迹调控区(imprinting control region,ICR)并调控印迹基因簇表达,印迹基因簇包含几个相邻的母系印迹和父系印迹基因。因此,印迹基因表达失调可能会影响胎儿正常发育,并导致人类疾病(如印迹综合征)。
尽管DNA甲基化已在基因组印迹背景下得到了广泛研究,但DNA羟甲基化在ICR调控中的作用及在印迹基因表达中的作用研究较少。研究表明,双Tet1/Tet2基因敲除小鼠在不同印迹位点表现出DNA甲基化变化。Tet1和Tet2参与细胞融合模型中基因组印记的有效敲除,通过将5mC转化为5hmC参与小鼠原始生殖细胞的印记敲除,表明5hmC在基因组印记中的敲除、建立和维持中起着关键作用。然而关于TET缺失在胎盘特异性印迹基因的作用机制尚不清楚。在TET1敲除小鼠精子父系表达基因(如Peg10和Peg3)的几个DMR表现出高甲基化模式,在Tet1敲除胎盘中Peg3 DMR高甲基化,表明TET1在父系印记敲除中起着关键作用。这导致了许多不同的表型,如胎盘、胎儿和出生后的生长缺陷以及早期胚胎致死性。
在人的胎盘中,印迹基因CDKN1C表达与出生体重和ICR调控CDKN1C表达的5hmC富集之间存在相关性。Hernandez-Mora等团队揭示了单等位基因5hmC在GNAS A/B DMR、H19基因体和几种胎盘特异性DMR(如MCCC1、RHOBTB3、SCIN、DNMT1和ACTL10)区域中的富集。一些在DMR中5hmC富集的基因与印迹疾病相关,因此对这些DMR中5hmC水平的研究具有特别的相关性。由于5hmC由先前甲基化DNA氧化产生,可能会出现仅在印迹DMR甲基化等位基因上存在5hmC的情况。
宫内生长受限(IUGR)中的DNA羟甲基化
宫内生长受限(intrauterine growth restriction,IUGR)是一种复杂而常见的产科并发症,并与围产期发病率和死亡率显著相关,主要在于胎儿无法实现其生长潜能。基于超声检测估计的胎儿长度,当低于胎龄第10百分位时,归类为IUGR。IUGR可能是母体、胎盘或胎儿的原因,其中营养和氧气运输不足导致的胎盘功能不全是主要原因之一。
目前的研究除了对IUGR胎盘中DNA甲基化的广泛研究外,还对IUGR胎盘中的DNA羟甲基化进行了分析(表1)。对单卵(monozygotic,MZ)双胞胎的研究对于理解妊娠并发症和人类疾病的表观遗传学基础具有重要价值。在MZ双胞胎选择性宫内生长受限(sIUGR)胎盘中揭示了全基因组DNA羟甲基化降低。Zhang等团队揭示了sIUGR妊娠中较小比例的胎盘中表现出全基因组5hmC水平降低,同时还表现出ANGPTL4和HIF1A基因启动子中5hmC水平较低,ANGPTL4和HIF1A基因为低氧响应基因,在小比例sIUGR胎盘中下降,可能是因为TET酶需要氧气将5mC氧化成5hmC。动物模型实验证据表明,子宫内缺氧导致胎儿生长受限。此外癌症研究表明,缺氧会影响TET酶的活性。对表观遗传调节因子在IUGR胎盘中的表达研究结果表明,TET3表达以及所有三种DNMT(DNMT1、DNMT3A和DNMT3B)上调,全基因组DNA甲基化或羟甲基化水平无变化。研究阐明了DNA羟甲基化在不协调胎儿生长甚至胎盘相关疾病中的潜在作用。
此外,还要考虑到环境条件可能会影响胎盘表观基因组并可能影响胎儿生长。大鼠实验表明,在妊娠期间给予低蛋白饮食或母体暴露于三氯乙烯(一种广泛存在的环境污染物)会导致5hmC水平失调,并与胎儿生长受限有关。在IUGR大鼠模型中,Wnt5启动子的Wnt2基因表达和5hmC水平降低,表明营养缺乏(最终导致IUGR)可能改变胎盘的表观遗传状态。同时,妊娠期间母体暴露于三氯乙烯对大鼠胎儿体重产生负面影响,并导致5hmC水平和Tet3表达增加。
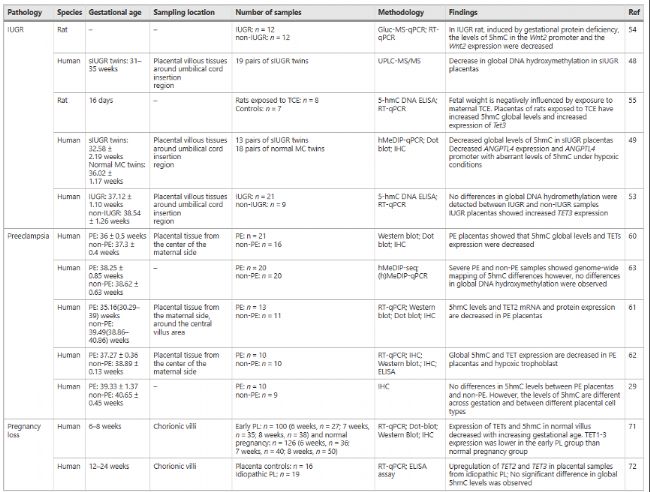 表1:胎盘DNA羟甲基化与妊娠并发症相关的研究,如宫内生长受限、子痫前期和妊娠丢失
表1:胎盘DNA羟甲基化与妊娠并发症相关的研究,如宫内生长受限、子痫前期和妊娠丢失
先兆子痫中的 DNA 羟甲基化
先兆子痫(preeclampsia,PE)是一种妊娠相关疾病,影响约3-5%的孕妇,其特征是先前血压正常的女性在20WG后出现高血压和蛋白尿,可能导致孕产妇、围产期和胎儿的死亡率和发病率,并与IUGR、胎盘早剥、早产和心血管疾病等长期并发症有关。
一些表观遗传变化与PE有关,如DNA甲基化和羟甲基化修饰。一项研究显示H19启动子区域的高甲基化导致早发性先兆子痫胎盘的mRNA表达降低,同时还表现出全基因组DNA甲基化水平和DNMT1甲基转移酶mRNA增加。近期一些研究还分析了PE胎盘中DNA羟甲基化水平(表1):Liu等团队研究结果表明了整体5hmC水平下降,与PE胎盘中TET1-3表达下降一致;其他研究也报道与对照组胎盘相比,PE胎盘中的全基因组5hmC水平较低,TET水平降低;Li等团队研究结果揭示了PE胎盘中5hmC水平和TET2转录本的降低,这与使用TET2 shRNA敲低细胞模型时获得的结果一致,TET2下调导致5hmC水平降低、滋养层迁移和侵袭减少,此外TET2下调抑制了MMP9表达,MMP9是一种血管生成相关蛋白,可以通过维生素C(TET酶活性激活剂)来挽救;Ma等团队研究表明,PE胎盘和低氧培养细胞中IGF1 mRNA和蛋白表达降低,低氧条件下培养的PE胎盘和滋养层细胞显示整体5hmC水平降低、整体5mC水平增加,5hmC降低与PE胎盘中TET表达降低结果一致;其他研究没有表明PE胎盘和无并发症妊娠胎盘之间5hmC整体水平的差异,尽管PE胎盘中5mC水平较高;Zhu等团队研究也没有揭示PE和非PE胎盘之间整体DNA羟甲基化水平和整体DNA甲基化水平的差异,但检测到与403个基因相关的714个DMR和与61个基因重叠的119个差异羟甲基化区域(DHMR)的位点特异性修饰;此外所研究的区域在5mC和5hmC中没有同时变化,突出表明两种表观遗传标记可能在迟发性严重PE中具有独立作用。
大多数使用斑点印迹(Dot blot)和IHC的研究揭示了PE样品中5hmC整体水平较低(表1),hMeDIP-Seq虽然描述了位点特异性差异,但并未检测到全基因组差异。尽管大多数研究都从母体分析了胎盘组织,但取样点也可能会干扰研究结果。
妊娠丢失中的DNA羟甲基化
妊娠丢失(pregnancy loss,PL,俗称流产)是最常见的产科并发症之一,具有很强的临床和社会影响。研究表明,早期妊娠丢失与较高的心理发病率之间存在关联,如抑郁、焦虑和创伤后应激症。约10-15%临床确认的妊娠终止于自然妊娠丢失。妊娠丢失可能是偶发性或复发性事件,约1-5%的病例为复发性妊娠丢失,这种临床并发症具有异质性病因,由几种已知的危险因素引起,如子宫解剖缺陷、免疫、感染、环境、内分泌、血栓形成和遗传因素,其中遗传因素被认为是导致妊娠丢失的主要原因,胎儿染色体异常占病例的50-60%。然而,相当大比例的复发性妊娠丢失具有正常的细胞核型和特发性。
由于胎盘在母体-胎儿交换和内分泌功能中发挥作用,胎盘发育和功能紊乱可能对胎儿产生负面影响,最终导致妊娠丢失。越来越多的证据表明,表观遗传功能障碍可能影响正常妊娠的稳定性,并导致妊娠期并发症(如IUGR和PE)。但TET酶功能失调和5hmC异常水平是否与可能导致妊娠丢失的异常胎盘功能有关仍不清楚(表1)。
Wu等团队对自然早期妊娠丢失(EPL)和正常妊娠(医学终止妊娠)绒毛膜绒毛中TET和5hmC水平表达进行研究,研究结果表明,EPL组绒毛中TET1、TET2和TET3表达低于正常妊娠组,6~8WG期间EPL组5hmC水平较低,但仅在6WG表达。此外TET和5hmC在正常绒毛中的表达随胎龄增加而降低。妊娠中期自然妊娠丢失的人胎盘中TETs表达和5hmC水平分析结果揭示了特发性(idiopathic)妊娠丢失胎盘组织的TET失调。然而在特发性病例胎盘样本12-24WG期间的TET2和TET3过表达。尽管TET2和TET3表达在特发性自然妊娠丢失的胎盘中上调,但整体DNA羟甲基化水平无统计学意义上的显著变化。在未来,分析特发性妊娠丢失的胎盘DNA特定基因组区域的5hmC水平很有必要(如5hmC富集的印迹基因调控区域)。
结论
胎盘对于支持妊娠期的胎儿发育至关重要。尽管单细胞RNA测序等新技术正在出现,并揭示了人类滋养层细胞的特异性表征,但研究人类胎盘的复杂性和胎盘发育的动态变化仍具有挑战性。胎盘发育异常是不同妊娠并发症的基础,因此详细理解调控滋养层细胞分化的分子机制有助于提高相关疾病的诊断和治疗。随着对表观遗传学机制的不断理解深入,尤其是DNA羟甲基化在正常和复杂妊娠的人类胎盘发育过程中可能发挥的作用,DNA羟甲基化可能是功能性胎盘发育的重要表观遗传机制。就这一点而言,胎盘研究具有十分重要的意义。
多项研究支持TET和5hmC在胎盘发育中的作用,当然还需要在体外和动物模型中进行功能研究,尤其是在胎盘中下调TET,以帮助阐明这些表观遗传修饰因子在胎盘细胞分化和功能中的作用。应进一步研究5hmC和TET在正常和病理性胎盘、特异性疾病(如IUGR、PE和妊娠丢失等)以及特异性基因组区域(调控基因区域、TSS或CpG岛)中的表达。这些研究将有助于增加知识,并可能有助于预防或更好地处理某些产科并发症。
参考文献:
Vasconcelos S, Caniçais C, Chuva de Sousa Lopes SM, Marques CJ, Dória S. The role of DNA hydroxymethylation and TET enzymes in placental development and pregnancy outcome. Clin Epigenetics. 2023 Apr 25;15(1):66.
胎盘是支持哺乳动物胚胎和胎儿发育所必需的临时器官。了解滋养层细胞分化和胎盘功能的分子机制可能有助于改善产科并发症的诊断和治疗。印迹基因是调控胎盘发育的基础,表观遗传学在基因表达(尤其是印迹基因)的调控中起着重要作用。TET酶(Ten-Eleven-Translocation enzymes)是表观遗传学机制的一部分,可以将5-甲基胞嘧啶(5mC)转化为5-羟甲基胞嘧啶(5hmC)。
DNA羟甲基化是DNA去甲基化机制中的中间体,并可能是一种稳定且功能相关的表观遗传学标记。DNA羟甲基化在胎盘分化和发育过程中的作用尚不完全清楚,但该领域知识的增加将有助于评估其在妊娠并发症中的潜在作用。本文综述了DNA羟甲基化及其表观遗传调控因子在人和小鼠胎盘发育和功能中的作用,并在基因组印迹机制和妊娠并发症(如宫内生长受限,先兆子痫和妊娠丢失)的背景下对5hmC进行探讨。累积的研究结果表明,DNA羟甲基化可能对调控胎盘中的基因表达非常重要,并提示在妊娠期间滋养层细胞分化中起着动态作用。
胎盘是由具有特殊功能的不同细胞类型组成的高度组织化器官,小鼠和人的胎盘发育在结构和分子水平上存在显著差异。在人胎盘发育过程中,单核细胞滋养层(cytotrophoblas,CTB)细胞向蜕膜间隙的迁移标志着初级胎盘绒毛形成的开始。这些CTB分化为绒毛外CTB,具有侵袭性并参与植入过程。此外,这些CTB还分化为绒毛CTB,融合并随后形成合胞体滋养层(syncytiotrophoblast,STB)细胞,在绒毛树表面形成连续的合胞体层,并与流经绒毛间隙的母体血液直接接触,从而实现母体-胎儿交换。在整个妊娠过程中,STB细胞通过持续融合初级CTB细胞来维持,因此在STB细胞内可以观察到不同程度染色质浓缩的细胞核形态。虽然大多数细胞核分散在合胞体内,但其他细胞核聚集在末端绒毛表面(合胞结)。因此,绒毛结构由包含胎儿血管的间充质核心、CTB层和STB外层组成(图1)。

图1:人胎盘
- 人胎盘结构(注:图纸不符合比例)。显示不同类型的细胞。
- 比较妊娠三个月的5hmC和TET水平。
- 比较滋养层细胞和合胞体滋养层细胞之间的5hmC水平。
绿色√标记:存在5hmC或表观遗传调控因子表达;红色X标记:不存在5hmC或表观遗传调控因子表达;绿色箭头⬆:5hmC或表观遗传调控因子水平增加;红色箭头⬇:5hmC或表观遗传调控因子水平降低;灰色方块:未研究
在小鼠中,胎儿-母体交换发生在与人绒毛胎盘类似的“迷宫(labyrinth)”中,其具有复杂的母体和胎儿血管通道序列。“迷宫”上方有一个由具有内分泌功能的滋养层巨细胞(trophoblast giant cell,TGC)、海绵滋养层细胞(spongiotrophoblast,SpT)和糖原滋养层细胞(glycogen trophoblast cell,GlyT)组成的结合区域(图2)。

图2:小鼠胎盘
- 小鼠胎盘结构
- 比较妊娠中期和妊娠晚期的5hmC和TET水平。
胎盘发育中的TET酶与DNA羟甲基化
TET酶参与胎盘滋养层细胞的分化和调控,5hmC水平失调导致胎盘异常发育。目前关于TET酶和DNA羟甲基化在胎盘发育中的作用研究有限。先前研究表明,胎盘基因组中的5hmC水平显著低于5mC水平。然而在以下两项研究中鉴定了CpG位点的存在,其5hmC水平持续增加,高于特定阈值且在样品之间可重复。Green等团队研究揭示了约21000个位点的5hmC平均值为13.73%,Mora等团队检测到约17000个CpG位点的5hmC富集。两项研究均揭示了5hmC在公海(基因组中分离的CpG)和大陆架(距离CpG岛2-4 kb)区域富集,而在CpG岛中缺失。另外还检测到5hmC在基因体、5’ UTR和3’UTR区域中富集,在近端启动子(距TSS约 200–1500 bp)和TSS区域缺失。Green等报告了稳定增强子中的富集和活性增强子内的缺失,而Mora等报告印迹基因(如GNAS和H19)和胎盘特异性DMR中的5hmC,通常与亲本等位基因5mC相关区域重叠。Green等研究表明,与活跃转录基因相比,转录失活基因中的5mC和5hmC水平均增加,其中5hmC与转录呈正相关。明显矛盾的研究结果可能归因于周转率的增加,周转率增加与在转录失活基因中观察到的甲基化水平增加有关,这些基因转化为羟甲基化水平增加。5hmC也更可能发生在妊娠中期和足月胎盘之间的差异表达基因中。
在人胎盘中,Fogarty等团队研究表明,与CTB细胞相比,5hmC在STB中更为富集,其中20–50%的STB细胞核在妊娠早期和中期呈阳性(positive),50%的STB细胞核在妊娠晚期呈阳性,尤其是在完全由5hmC阳性细胞核组成的合胞结中。相比之下,大多数STB细胞核在妊娠期间的5mC染色水平不显著,而超50%的CTB细胞核为5mC阳性(28)。Wilson等团队使用免疫荧光法分析结果表明,与妊娠早期和中期胎盘相比,足月胎盘的CTB和STB细胞中5hmC(和5mC)均增加(图1B)。在妊娠早期和中期,STB细胞中的5hmC染色更为显著(图1C)。在整个妊娠期间,随着CTB融合产生STB,STB中可能沉积5hmC,尤其在合胞结中,可能表明结形成过程中发生的氧化损伤。这些结果表明两种细胞类型之间的差异可能揭示其不同功能。例如绒毛滋养层细胞调节气体和营养交换,而STB在整个妊娠期间产生和分泌大量激素,揭示了该组织的高转录和翻译能力。如Rouault等团队研究结果揭示了CTB和STB的特异性转录组谱。
在小鼠胎盘中,在胚胎期(E)第8.5天,小鼠胎盘外胎盘锥体细胞(ectoplacental cone cell,EPC)和顶叶TGC(parietal-TGC)表现出5hmC高水平和5mC低水平。E10.5-E18.5期间所有“迷宫”细胞中维持细胞核内5mC水平,STB细胞核在整个妊娠期间呈现出5mC高水平。在E10.5时,所有“迷宫”滋养层细胞中均表现出5hmC高水平,但E18.5时水平逐渐降低。顶叶TGC在5hmC中逐渐降低,但5mC水平在E18.5时稳定增加(图2B)。总之,这些研究强调了不同滋养层细胞来源细胞类型的表观基因组动态变化,且在妊娠期间发生变化。
另一方面,关于TET酶在滋养层细胞分化过程中的作用研究较少。TET酶的敲低模型表明,5hmC对于维持发育和早期胚胎发生至关重要。Yamaguchi等团队研究表明,与对照组相比,父系TET1-KO小鼠可导致包括胎盘缺陷在内的多种表型,父系TET1-KO小鼠的胎盘显著缩小。Rakoczy等团队研究了TET酶在小鼠和人胎盘中的表达,小鼠中Tet1、Tet2和Tet3 mRNA在E8.5的绒毛膜、EPC和卵黄囊中表达,在E10.5~E12.5的“迷宫”(包括窦性TGC和STB细胞)中表达。而Tet1-3只在E14.5~E18.5的窦性TGC中表达,在STB中Tet不表达,这与妊娠晚期STB中观察到的5hmC水平一致。对于SpT细胞,Tet1-3在整个妊娠期间持续表达,而在GlyT细胞中仅在E14.5-E16.5之间显著强表达。除E10.5和E18.5分别出现Tet1表达缺失和Tet3表达降低外,顶叶TGC在整个妊娠期间的所有TET中均表达(图2B)。因此在E18.5时,顶叶TGC中5hmC水平降低与Tet3表达下调结果一致。在人胎盘的妊娠早期和晚期的STB细胞中检测到TET1-3蛋白,但在妊娠8周(weeks of gestation,WG)时除外(TET1未检测到)。绒毛CTB细胞在妊娠早期和晚期TET1和TET2不表达,TET3从10WG~足月期间均表达(图1B)。这些研究结果表明TET1和TET2在STB分化中起着重要作用。与CTB仅TET3表达相比,STB中5hmC的较高水平可能是三种TET在STB均表达的结果。由于胎盘发育是一个高度动态的过程,因此研究这些酶在妊娠中期胎盘中的表达也很重要。
关于TET酶的非催化作用,TET酶与一些表观遗传修饰因子(如组蛋白修饰酶)相互作用,导致TET靶向基因的抑制。如有研究表明TET1和EZH2之间的相互作用,它负责调控H3K27me3(一种在CTB细胞核中的组蛋白标记)和其他组蛋白修饰。
虽然胎盘结构在不同细胞类型中存在差异,但在妊娠期间的人和小鼠滋养层细胞中观察到5mC和5hmC以及TET表达。在妊娠末期可能会出现STB异常,因为在小鼠中TET不表达,但在人胎盘中TET表达。整个妊娠期间,在人类中5hmC水平增加,而在小鼠中5hmC降低。当然,还需要更多的研究来证实小鼠和人类之间的差异,并阐明其在胎盘发育过程中在细胞调控和分化中的作用。
胎盘印记基因中的DNA羟甲基化
1984年的细胞核移植实验首次描述了基因组印迹,带有两组母系染色体(雌核发育(gynogenotes))或两组父系染色体(雄核发育(androgenote))的小鼠胚胎无法正常发育,前者表现为胚胎外组织(胎盘和卵黄囊)生长迟缓和异常发育,后者表现为胚胎外组织过度生长和胚胎本身发育不良。实验结果表明尽管遗传信息相似,但遗传的母系和父系染色体在功能上并不相同。基因组印迹是一种表观遗传机制,其中印迹基因表现为单等位基因和亲本依赖性表达,受DNA差异甲基化区域(DMR)调控。其中一些DMR充当印迹调控区(imprinting control region,ICR)并调控印迹基因簇表达,印迹基因簇包含几个相邻的母系印迹和父系印迹基因。因此,印迹基因表达失调可能会影响胎儿正常发育,并导致人类疾病(如印迹综合征)。
尽管DNA甲基化已在基因组印迹背景下得到了广泛研究,但DNA羟甲基化在ICR调控中的作用及在印迹基因表达中的作用研究较少。研究表明,双Tet1/Tet2基因敲除小鼠在不同印迹位点表现出DNA甲基化变化。Tet1和Tet2参与细胞融合模型中基因组印记的有效敲除,通过将5mC转化为5hmC参与小鼠原始生殖细胞的印记敲除,表明5hmC在基因组印记中的敲除、建立和维持中起着关键作用。然而关于TET缺失在胎盘特异性印迹基因的作用机制尚不清楚。在TET1敲除小鼠精子父系表达基因(如Peg10和Peg3)的几个DMR表现出高甲基化模式,在Tet1敲除胎盘中Peg3 DMR高甲基化,表明TET1在父系印记敲除中起着关键作用。这导致了许多不同的表型,如胎盘、胎儿和出生后的生长缺陷以及早期胚胎致死性。
在人的胎盘中,印迹基因CDKN1C表达与出生体重和ICR调控CDKN1C表达的5hmC富集之间存在相关性。Hernandez-Mora等团队揭示了单等位基因5hmC在GNAS A/B DMR、H19基因体和几种胎盘特异性DMR(如MCCC1、RHOBTB3、SCIN、DNMT1和ACTL10)区域中的富集。一些在DMR中5hmC富集的基因与印迹疾病相关,因此对这些DMR中5hmC水平的研究具有特别的相关性。由于5hmC由先前甲基化DNA氧化产生,可能会出现仅在印迹DMR甲基化等位基因上存在5hmC的情况。
宫内生长受限(IUGR)中的DNA羟甲基化
宫内生长受限(intrauterine growth restriction,IUGR)是一种复杂而常见的产科并发症,并与围产期发病率和死亡率显著相关,主要在于胎儿无法实现其生长潜能。基于超声检测估计的胎儿长度,当低于胎龄第10百分位时,归类为IUGR。IUGR可能是母体、胎盘或胎儿的原因,其中营养和氧气运输不足导致的胎盘功能不全是主要原因之一。
目前的研究除了对IUGR胎盘中DNA甲基化的广泛研究外,还对IUGR胎盘中的DNA羟甲基化进行了分析(表1)。对单卵(monozygotic,MZ)双胞胎的研究对于理解妊娠并发症和人类疾病的表观遗传学基础具有重要价值。在MZ双胞胎选择性宫内生长受限(sIUGR)胎盘中揭示了全基因组DNA羟甲基化降低。Zhang等团队揭示了sIUGR妊娠中较小比例的胎盘中表现出全基因组5hmC水平降低,同时还表现出ANGPTL4和HIF1A基因启动子中5hmC水平较低,ANGPTL4和HIF1A基因为低氧响应基因,在小比例sIUGR胎盘中下降,可能是因为TET酶需要氧气将5mC氧化成5hmC。动物模型实验证据表明,子宫内缺氧导致胎儿生长受限。此外癌症研究表明,缺氧会影响TET酶的活性。对表观遗传调节因子在IUGR胎盘中的表达研究结果表明,TET3表达以及所有三种DNMT(DNMT1、DNMT3A和DNMT3B)上调,全基因组DNA甲基化或羟甲基化水平无变化。研究阐明了DNA羟甲基化在不协调胎儿生长甚至胎盘相关疾病中的潜在作用。
此外,还要考虑到环境条件可能会影响胎盘表观基因组并可能影响胎儿生长。大鼠实验表明,在妊娠期间给予低蛋白饮食或母体暴露于三氯乙烯(一种广泛存在的环境污染物)会导致5hmC水平失调,并与胎儿生长受限有关。在IUGR大鼠模型中,Wnt5启动子的Wnt2基因表达和5hmC水平降低,表明营养缺乏(最终导致IUGR)可能改变胎盘的表观遗传状态。同时,妊娠期间母体暴露于三氯乙烯对大鼠胎儿体重产生负面影响,并导致5hmC水平和Tet3表达增加。
 表1:胎盘DNA羟甲基化与妊娠并发症相关的研究,如宫内生长受限、子痫前期和妊娠丢失
表1:胎盘DNA羟甲基化与妊娠并发症相关的研究,如宫内生长受限、子痫前期和妊娠丢失先兆子痫中的 DNA 羟甲基化
先兆子痫(preeclampsia,PE)是一种妊娠相关疾病,影响约3-5%的孕妇,其特征是先前血压正常的女性在20WG后出现高血压和蛋白尿,可能导致孕产妇、围产期和胎儿的死亡率和发病率,并与IUGR、胎盘早剥、早产和心血管疾病等长期并发症有关。
一些表观遗传变化与PE有关,如DNA甲基化和羟甲基化修饰。一项研究显示H19启动子区域的高甲基化导致早发性先兆子痫胎盘的mRNA表达降低,同时还表现出全基因组DNA甲基化水平和DNMT1甲基转移酶mRNA增加。近期一些研究还分析了PE胎盘中DNA羟甲基化水平(表1):Liu等团队研究结果表明了整体5hmC水平下降,与PE胎盘中TET1-3表达下降一致;其他研究也报道与对照组胎盘相比,PE胎盘中的全基因组5hmC水平较低,TET水平降低;Li等团队研究结果揭示了PE胎盘中5hmC水平和TET2转录本的降低,这与使用TET2 shRNA敲低细胞模型时获得的结果一致,TET2下调导致5hmC水平降低、滋养层迁移和侵袭减少,此外TET2下调抑制了MMP9表达,MMP9是一种血管生成相关蛋白,可以通过维生素C(TET酶活性激活剂)来挽救;Ma等团队研究表明,PE胎盘和低氧培养细胞中IGF1 mRNA和蛋白表达降低,低氧条件下培养的PE胎盘和滋养层细胞显示整体5hmC水平降低、整体5mC水平增加,5hmC降低与PE胎盘中TET表达降低结果一致;其他研究没有表明PE胎盘和无并发症妊娠胎盘之间5hmC整体水平的差异,尽管PE胎盘中5mC水平较高;Zhu等团队研究也没有揭示PE和非PE胎盘之间整体DNA羟甲基化水平和整体DNA甲基化水平的差异,但检测到与403个基因相关的714个DMR和与61个基因重叠的119个差异羟甲基化区域(DHMR)的位点特异性修饰;此外所研究的区域在5mC和5hmC中没有同时变化,突出表明两种表观遗传标记可能在迟发性严重PE中具有独立作用。
大多数使用斑点印迹(Dot blot)和IHC的研究揭示了PE样品中5hmC整体水平较低(表1),hMeDIP-Seq虽然描述了位点特异性差异,但并未检测到全基因组差异。尽管大多数研究都从母体分析了胎盘组织,但取样点也可能会干扰研究结果。
妊娠丢失中的DNA羟甲基化
妊娠丢失(pregnancy loss,PL,俗称流产)是最常见的产科并发症之一,具有很强的临床和社会影响。研究表明,早期妊娠丢失与较高的心理发病率之间存在关联,如抑郁、焦虑和创伤后应激症。约10-15%临床确认的妊娠终止于自然妊娠丢失。妊娠丢失可能是偶发性或复发性事件,约1-5%的病例为复发性妊娠丢失,这种临床并发症具有异质性病因,由几种已知的危险因素引起,如子宫解剖缺陷、免疫、感染、环境、内分泌、血栓形成和遗传因素,其中遗传因素被认为是导致妊娠丢失的主要原因,胎儿染色体异常占病例的50-60%。然而,相当大比例的复发性妊娠丢失具有正常的细胞核型和特发性。
由于胎盘在母体-胎儿交换和内分泌功能中发挥作用,胎盘发育和功能紊乱可能对胎儿产生负面影响,最终导致妊娠丢失。越来越多的证据表明,表观遗传功能障碍可能影响正常妊娠的稳定性,并导致妊娠期并发症(如IUGR和PE)。但TET酶功能失调和5hmC异常水平是否与可能导致妊娠丢失的异常胎盘功能有关仍不清楚(表1)。
Wu等团队对自然早期妊娠丢失(EPL)和正常妊娠(医学终止妊娠)绒毛膜绒毛中TET和5hmC水平表达进行研究,研究结果表明,EPL组绒毛中TET1、TET2和TET3表达低于正常妊娠组,6~8WG期间EPL组5hmC水平较低,但仅在6WG表达。此外TET和5hmC在正常绒毛中的表达随胎龄增加而降低。妊娠中期自然妊娠丢失的人胎盘中TETs表达和5hmC水平分析结果揭示了特发性(idiopathic)妊娠丢失胎盘组织的TET失调。然而在特发性病例胎盘样本12-24WG期间的TET2和TET3过表达。尽管TET2和TET3表达在特发性自然妊娠丢失的胎盘中上调,但整体DNA羟甲基化水平无统计学意义上的显著变化。在未来,分析特发性妊娠丢失的胎盘DNA特定基因组区域的5hmC水平很有必要(如5hmC富集的印迹基因调控区域)。
结论
胎盘对于支持妊娠期的胎儿发育至关重要。尽管单细胞RNA测序等新技术正在出现,并揭示了人类滋养层细胞的特异性表征,但研究人类胎盘的复杂性和胎盘发育的动态变化仍具有挑战性。胎盘发育异常是不同妊娠并发症的基础,因此详细理解调控滋养层细胞分化的分子机制有助于提高相关疾病的诊断和治疗。随着对表观遗传学机制的不断理解深入,尤其是DNA羟甲基化在正常和复杂妊娠的人类胎盘发育过程中可能发挥的作用,DNA羟甲基化可能是功能性胎盘发育的重要表观遗传机制。就这一点而言,胎盘研究具有十分重要的意义。
多项研究支持TET和5hmC在胎盘发育中的作用,当然还需要在体外和动物模型中进行功能研究,尤其是在胎盘中下调TET,以帮助阐明这些表观遗传修饰因子在胎盘细胞分化和功能中的作用。应进一步研究5hmC和TET在正常和病理性胎盘、特异性疾病(如IUGR、PE和妊娠丢失等)以及特异性基因组区域(调控基因区域、TSS或CpG岛)中的表达。这些研究将有助于增加知识,并可能有助于预防或更好地处理某些产科并发症。
参考文献:
Vasconcelos S, Caniçais C, Chuva de Sousa Lopes SM, Marques CJ, Dória S. The role of DNA hydroxymethylation and TET enzymes in placental development and pregnancy outcome. Clin Epigenetics. 2023 Apr 25;15(1):66.





