开启2020年科研新热点的染色体外环状DNA(eccDNA)
文章导读
近期,Nature与Cell相继发表文章讨论染色体外环状DNA(eccDNA),这位超级明星在各家媒体、宣传号上纷纷闪亮登场。一时间eccDNA走在了生物医学研究舞台的最中央,云序生物已经带您领略过eccDNA在这两篇重量级文章中的迷人风采(点击链接:颠覆性发现:癌基因竟不在染色体上---环状DNA连登Nature,Cell!),它极大的丰富了肿瘤异质性的研究内容,为液体活检、肿瘤耐药以及肿瘤微环境讨论指明了新的方向。eccDNA在肿瘤环境中可以借助多样的成环方式、开放的高级结构以及多个调控元件的辅助,强有力的推动原癌基因的转录,颠覆了科研人员对原癌基因在肿瘤发生发展当中的传统认知。染色质是动态的!eccDNA也是动态的!
虽然eccDNA的讨论内容多数围绕肿瘤环境,那eccDNA是否是肿瘤学的专属明星分子?并非如此,非疾病状态下的细胞核同样拥有丰富的eccDNA。云序生物今天带来的文章将让大家感受到,eccDNA在正常的人体细胞中(组织、血液)依旧存在,DNA的成环现象非常普遍。

原文链接:Circular DNA elements of chromosomal origin are common in healthy human somatic tissue
发表期刊:Nature Communication
影响因子:11.878
发表日期: 2018.08
实验方法:eccDNA-seq RNA-seq(云序生物提供以上服务)
文章内容
1. eccDNA成环的整体统
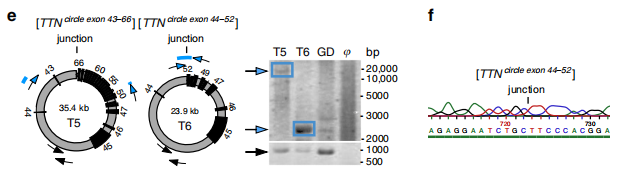
图1 来源于TNN基因的两例eccDNA
2.eccDNA长度分布与来源探索
eccDNA是环状结构,这样一种分子的长度分布如何?测序结果显示99%的eccDNA长度小于25Kb,其中仅有占比约1%的分子大于25Kb。在这99% 当中,在0.1Kb以及5Kb处有富集峰,这表明该区段的eccDNA占绝大多数。经典的知识体系告诉我们重复序列以及5sRNA部分最容易成环,事实上测序结果也充分证明这一点,SINE(3.1%)、LINE(3.5%),中心粒(2.0%),以及sRNA(8.1%)部分是最经典的成环结构,大量的环能够匹配到这些区域。
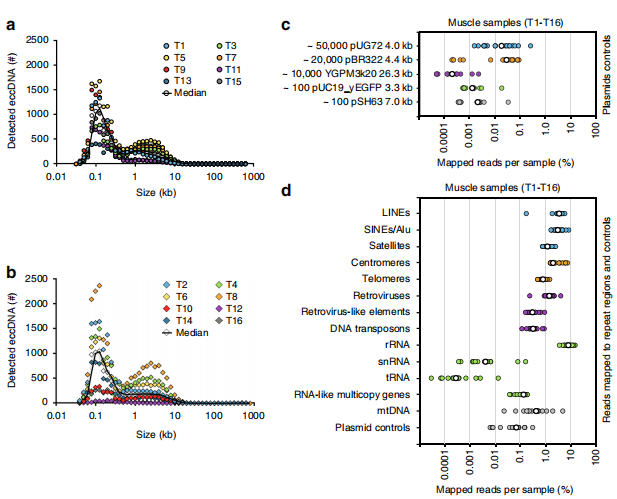
图2 eccDNA长度分布和来源多样性
3.eccDNA基因组分布
前文提到99% eccDNA小于25Kb,作者分别探索这些eccDNA来源于哪些染色体。结果显示所有染色体对eccDNA都有所贡献。其中小于25Kb部分的环状在染色体上的分布相对密集。

图3 eccDNA的染色体分布
4. eccDNA形成的基因偏好性
既然每一条染色体都有可能成环,都对eccDNA多样性产生巨大贡献,那eccDNA产生是否有一定的偏好性呢?文章测序结果显示17和19号染色体成环的可能性最大,由于17号染色体有相对多的编码基因,研究者猜测成环的可能性可能与编码基因数目呈正相关。
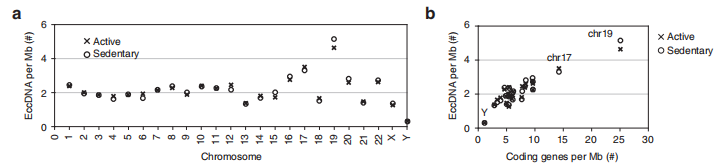
图4 17号与19号染色体对eccDNA贡献最大
5. eccDNA具有转录活性
eccDNA能够高效扩增成环序列,这种扩增是否有转录活性?RNA转录本是否仅仅来源于传统线性的染色体?要回答这一问题,作者通过RNA-seq(云序提供该服务)进行探索,结果发现split-reads,即在RNA-seq测序的结果当中同样发现了能够跨过相同剪切位点的测序片段,这种片段的剪切位点和eccDNA成环的剪切位点序列保持一致,说明环形的eccDNA也具有转录活性,这一点非常重要,这很有可能造成成环基因(尤其原癌基因和耐药基因)在转录本水平的明显高表达从而进一步促进癌症的发生发展,是非常具有临床意义的研究成果。
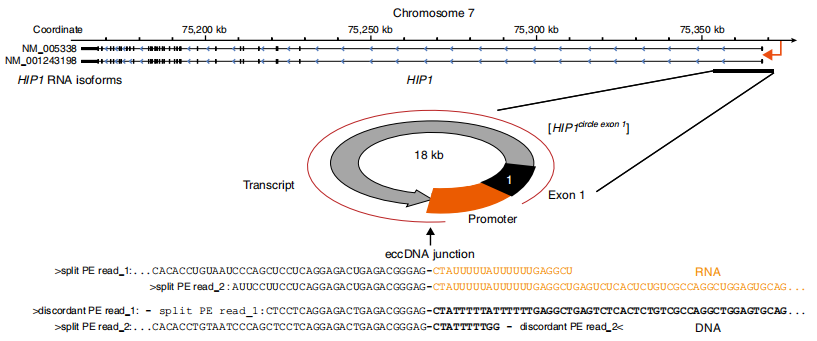
图5 HIP1形成eccDNA具有转录活性
6. eccDNA成环验证
类比于经典的circRNA,eccDNA的形成具有相似性,也是经过核酸序列的反式链接得到的产物。当然有关于成环机制的问题依然还需要大量的研究讨论。不过对于环状的结构验证可以模仿circRNA,针对junction site,就是链接位点设计发散引物(divergent primer)同时设计收敛引物(convergent primer)进行PCR扩增,然后通过Sanger测序的方式验证eccDNA的接头序列。
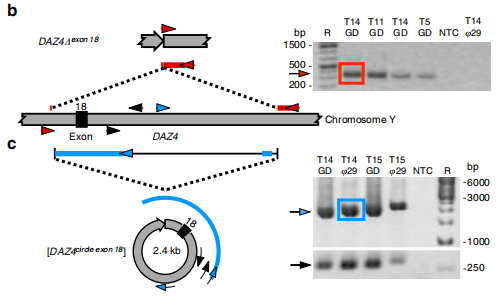
图6 eccDNA的验证
总结
从eccDNA全新视角理解生物过程的发生发展,这篇Nature Communication文章提供了最好的参照。研究者在进行eccDNA-seq之后对高通量数据进行整理归纳,从eccDNA的个数、长度、来源、分布和基因相关性进行深入分析,造就一篇10分以上“表达谱”的文章。这将会是一个契机,通过快速的eccDNA-seq结合PCR方式率先用“谱”的方式快速阐述一个疾病当中哪些基因易于成环、哪些基因扩增效率更高并快速和疾病的发生发展建立联系,有理由相信这种虽然简单但是高度创新的文章一定会备受瞩目,影响因子再创新高。
eccDNA以颠覆传统认知的方式重新走到科研舞台的中心,必将在未来的一段时间掀起一场有关基因扩增、转录的大讨论。我们已经习惯了观察基因的缺失、突变、插入和移位,eccDNA的产生从新的角度让科研工作者去思考基因组存在的动态性和多样性。由此,肿瘤的异质性、肿瘤微环境、液体活检和耐药性等相关研究必定会围绕eccDNA展开更多集中式的研究和探索,有理由相信这次2019年年末的Nature和Cell文章的发表将成为里程碑式的作品,引领未来三到五年内有关eccDNA研究的新方向。
云序生物作为高通量技术科研服务产品推广的先行者,向各位研究者隆重推荐最新eccDNA-seq产品,该产品做为业内率先发布的eccDNA测序服务,紧扣科研时代脉搏,紧跟前沿步伐,更快、更好、更新的满足科研工作者在自己研究领域内对于eccDNA的探索,欢迎新老客户来电咨询。
云序生物染色体外环状DNA测序技术服务:
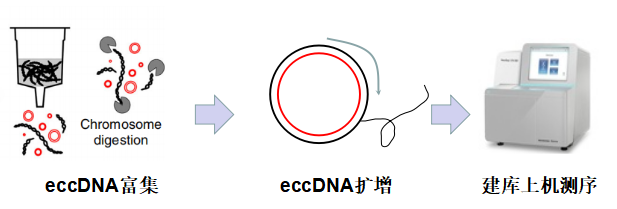
云序生物提供染色体外环状DNA测序服务(eccDNA-seq),利用核酸酶对线性DNA水解获得纯净的环状DNA,不仅检测到的有效数据量高,还能够深入分析在特定肿瘤癌症中相关eccDNA的特异表达、基因组分布以及拷贝变异等,从而帮助客户快速找到癌症、肿瘤机理研究和诊断的靶向eccDNA。
云序优势
国内率先提供该服务的测序公司:
通过长期的摸索,率先开发出成熟的测序流程,成为国内目前率先提供该服务的测序公司。
富集效率高:
染色体外环状DNA的富集效率是决定数据质量的关键,云序生物精心优化和研发的实验流程,具有极高的富集效率和特异性。
识别率高:
专业的生物信息学团队,通过优化的算法能够高效识别染色体外环状DNA。
一站式服务:
客户只需提供细胞、组织或基因组DNA,云序生物为您完成从样品准备、环状DNA富集、文库制备、上机测序到数据分析的整套服务流程。
云序生物相关产品推荐
云序生物往期回顾
颠覆性发现:癌基因竟不在染色体上---环状DNA连登Nature,Cell!
circRNA和m6A再次秀恩爱携手登上Nature Communication
“雨露均沾”---- RNA甲基化“搭讪”成熟miRNA又出新花样
胖纸的福音!敲除Zfp217基因可通过RNA m6A带走你腰间的“救生圈”
占领C位!云序生物解析如何做到快速同时检测各类癌症当中RNA甲基化相关酶&RNA甲基化水平(下)
Nature | SMAD2/3与TGF-β通路协同影响转录因子发生m6A RNA甲基化调控干细胞发育
Nat. commun | Mettl3介导的m6A RNA甲基化调控骨髓间充质干细胞和骨质疏松症的命运
Nature | m6A RNA甲基化识别蛋白YTHDF1参与记忆的形成
RNA甲基化已经火成这样子了,你还在等什么!云序生物最新m6A“RNA甲基化”研究汇总—癌症篇
Genome research:不同RNA m5C甲基化修饰存在巨大差异
上海云序生物科技有限公司
Shanghai Cloud-seq Biotech Co., Ltd.
地址:上海市松江区莘砖公路 518 号 20 号楼 3 楼
电话:021-64878766
传真:021-64878766
网址:www.cloud-seq.com.cn
邮箱:market@cloud-seq.com.cn





