机械拉伸通过机械激活的阳离子通道 Piezo1 促进增生性瘢痕形成
增生性瘢痕 (HS) 形成是一种皮肤纤维增生性疾病,发生在皮肤损伤之后,导致严重的功能和审美障碍。迄今为止,已经建立了许多用于抑制 HS 形成的治疗方法,但其中很少有令人满意的结果。
近年来,研究表明,Piezo1 与细胞外机械微环境发生积极的相互作用,以确定细胞行为或疾病进展。因此,Piezo1 可能是调节力学介导的细胞行为和疾病的关键因素。
同样,疤痕形成的主要特征是 ECM 的积累,最终导致基质硬度的增加。更硬的疤痕组织建立了一个“恶性反馈循环”,不断刺激成纤维细胞的过度活化和胶原蛋白的产生,进一步促进 HS 的发展和收缩。然而,尚不清楚瘢痕中异常的机械微环境是否与 Piezo1 的机械感觉功能相互作用,以调节皮肤成纤维细胞的活性,最终导致HS 的形成。
以此为基点, 来自上海交通大学医学院附属第九人民医院、附属新华医院整形外科的专家学者进行了相关研究,在Cell Death & Disease 上发表了题为《Mechanical stretch promotes hypertrophic scar formation through mechanically activated cation channel Piezo1》的研究论文。
该实验使用体外牵张应力加载系统将循环机械拉伸应力(CMS)应用于HDFs。HDFs在培养板上以2×105细胞/ml培养。拉伸组以正弦模式应用CMS,振幅为10%,频率为0.5 Hz,静态组细胞在同一类型的培养皿中培养,但保持静止,两组在同一培养箱中培养。
首先,实验通过免疫组织化学分析证实人HS 组织中 Piezo1 水平升高;通过免疫荧光分析观察到 Piezo1 的表达与 HS 组织中的 α-SMA 水平相关,表明 Piezo1 在人 HS 组织中肌成纤维细胞中高表达。此外研究了牵张力诱导的HS 大鼠尾模型中 Piezo1 的表达,显示 Piezo1 在整个大鼠 HS 真皮中过表达。总之,这些结果证实Piezo1 可能与 HS 形成有关。
为了研究 HS 组织增加的基质硬度是否影响 Piezo1 的上调,实验建立了一个 CMS 模型来模拟 HS 发展过程中增加的组织硬化。首先检测了在不同强度拉伸下 HDFs 中 Piezo1 的蛋白质水平(图1 A、B)。
值得注意的是,发现 Piezo1 的表达因拉伸强度增加而上调。此外,当施加 10% 的拉伸强度时,Piezo1 的表达也会随着时间的推移而增加。这些发现表明 CMS 以时间和强度依赖性方式显著提高了HDFs中的 HDF 中 Piezo1 的表达。
此外,测试了 Piezo1 的活性是否影响 HDFs 中的钙内流。结果表明,CMS促进了负载Ca2+敏感荧光染料 (Fluo-8) 的HDFs中细胞内的钙浓度。重要的是,GsMTx4 处理或 Piezo1 敲低抑制了由 CMS 诱导的 HDFs 细胞内钙的积累,表明 Piezo1 介导了暴露于 CMS 的 HDFs 中的钙内流(图1 E-H)。总之,这些结果表明 CMS 可能促进 Piezo1 的过表达和 Piezo1 介导的 HDF 中的钙内流。
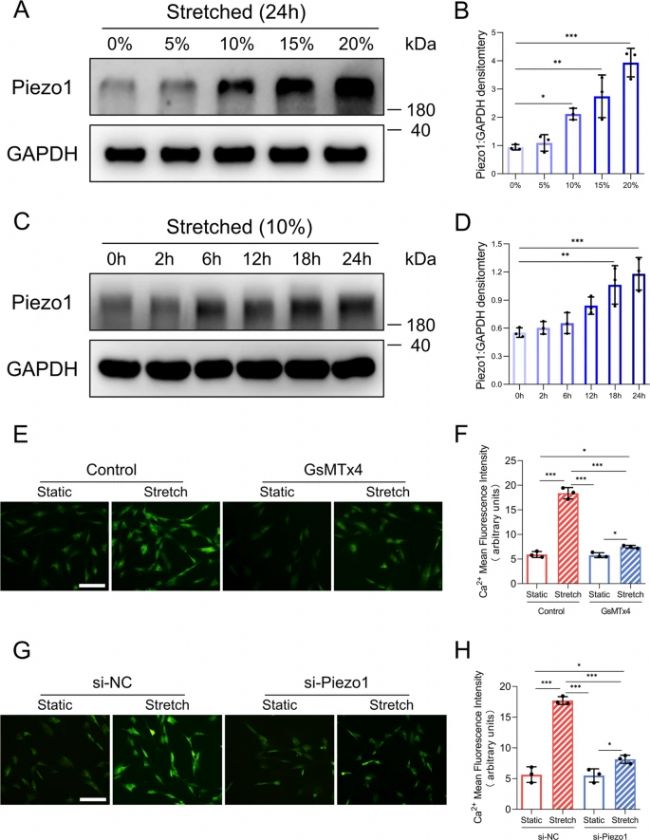
图1
此外,实验通过免疫荧光染色和Transwell 迁移测定,表明 Piezo1 可能参与机械拉伸诱导的 HDFs 的增殖和运动。
最后,实验检测了在大鼠拉伸诱导的瘢痕形成模型中GsMTx4 处理的效果。结果表明连续的机械拉伸作用于创口部位可以通过Piezo1 引起HS的形成。

总之,结果证实 Piezo1 激活可能介导 HS 的形成,并且可能成为治疗 HS 形成有希望的疗法新目标。研究结果还表明,Piezo1 阻断肽 GsMTx4 的应用也可能是一种治疗HS的潜在策略。更广泛地说,研究结果提出了一种可能性,即 Piezo1 可能是导致疾病的一般因素,而异常的机械力涉及其中。





