皮质纹状体谷氨酸介导的电针在帕金森病大鼠模型中的动态治疗效果
运动障碍是帕金森病 (PD) 的定义性主要特征,由皮质基底神经节回路功能障碍引起。临床数据表明,电针 (EA) 刺激可能有益于 PD 患者的运动症状,而没有不良反应。然而,EA 对 PD 的具体影响和潜在机制在很大程度上仍不清楚。
本研究调查了 100 Hz 应用期间和之后 EA 刺激对单侧注射 6-羟基多巴胺 (6-OHDA) 创建的 PD 大鼠模型的影响。为了建立 EA 的最佳治疗参数,研究员们使用旷场和旋转测试动态评估运动行为。此外,他们还使用免疫电子显微镜评估了皮质纹状体脊柱的可塑性,并通过微透析、体内电化学和高效液相色谱法测量了多巴胺能和谷氨酸能神经递质的水平。

本研究通过使用Cerebus在体多通道神经信号采集系统(Blackrock Mircosystems)采集了运动皮层和纹状体中的局部场电位来记录神经活动动力学。此外,还采用化学遗传学技术来探测皮质纹状体谷氨酸能神经元,并阐明在 PD 大鼠模型中导致 EA 治疗益处的机制。
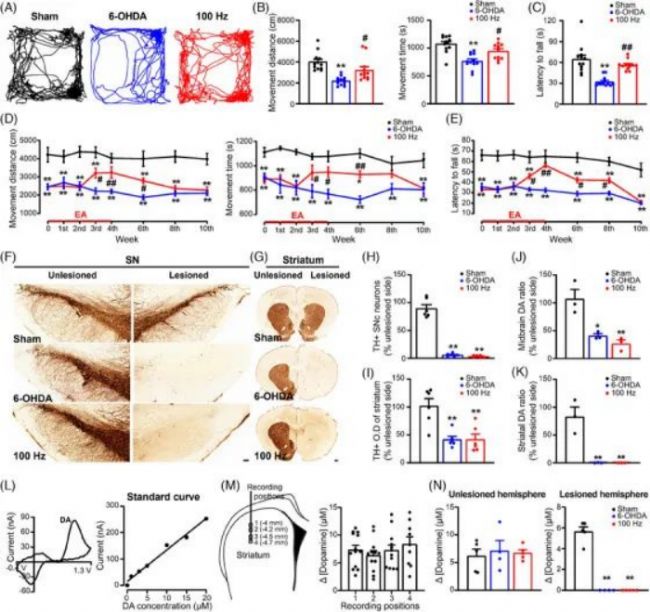
为了检查 EA 对运动症状的影响,研究员们最初评估了 PD 大鼠模型中的运动障碍。2 周后,由 6-OHDA 诱导病变的大鼠在旋转试验中表现出运动、行进距离更短和性能受损,表现出明显的运动障碍。接下来,研究员们研究了不同频率的 EA 刺激对 6-OHDA 损伤大鼠的影响。
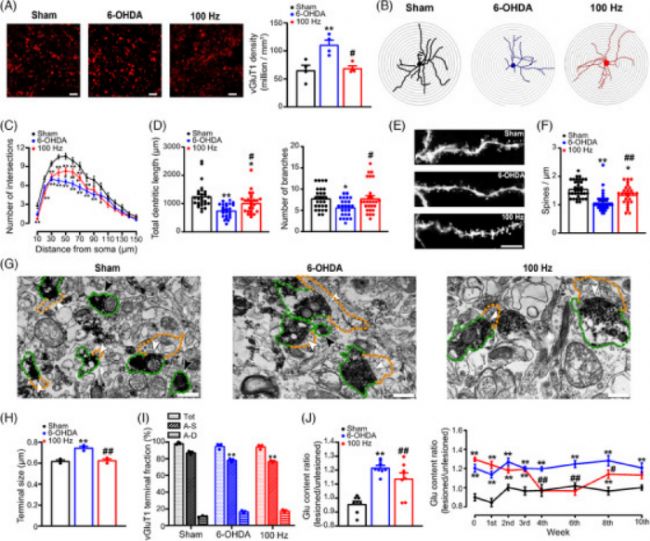
由于纹状体不仅接受黑质纹状体 DA能投射,还接受皮质纹状体和丘脑纹状体谷氨酸能输入,研究员们评估了 EA 治疗对 DA 耗竭后谷氨酸能投射的影响。为了实现这一目标,他们首先评估了 vGluT1 和 vGluT2 的密度,它们作为投射到纹状体的皮质和丘脑谷氨酸能轴突末端的标志物。
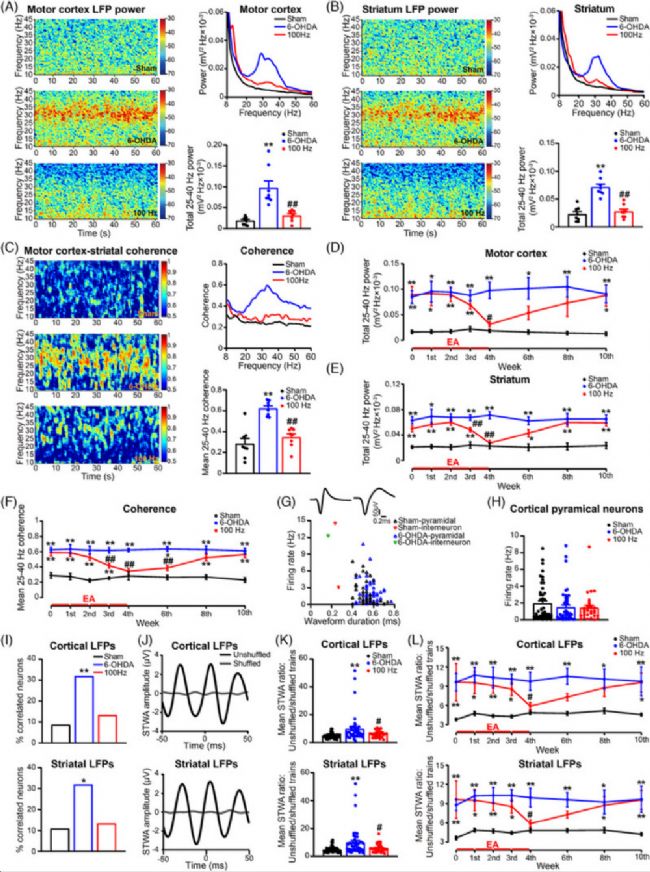
为了进一步评估 EA 刺激的动态治疗效果,研究员们在运动皮层和背外侧纹状体中使用长期植入的电极进行了同步记录。观察到DA 耗竭导致在纹状体和运动皮层中观察到的高β振荡幅度显著升高。皮质纹状体相干性在高β范围内也有所增加。
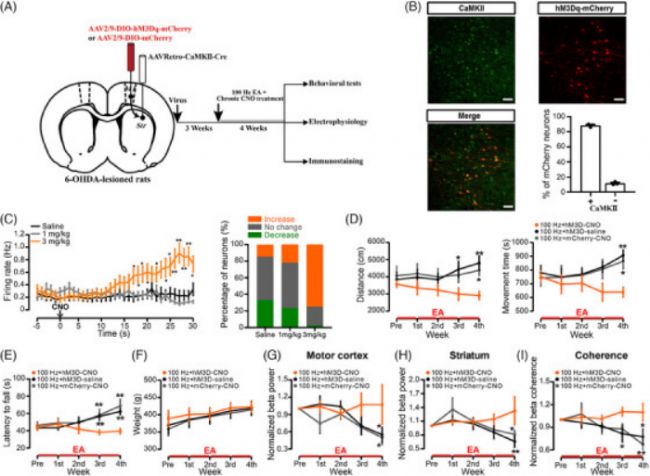
为了实现对抑制皮质纹状体神经元的选择性抑制,研究员们在 6-OHDA 损伤大鼠中使用了由设计药物 (DREADD) hM4Di 独家激活的抑制性设计受体。进行αCaMKII 和 hM4Di-mCherry 标记的免疫染色以验证细胞特异性。

为了进一步阐明皮质纹状体谷氨酸能传递对 6-OHDA 病变大鼠 EA 治疗效果的贡献,研究员们试图通过长期施用 CNO 激活 hM3Dq-DREADD 来抵消 EA 的影响。
越来越多的证据表明,EA 刺激通过多种方法对多巴胺能神经元提供神经保护作用。这些作用包括抗神经炎症、抗氧化应激和抗凋亡反应,以及调节肠道微生物组。

总之,本文的研究阐明了 PD 中 EA 治疗的时间动力学和最佳参数,它强调了抑制皮质纹状体谷氨酸传递在 EA 对 PD 的治疗益处中的重要性。
笔名:Liushuai
原文链接:https://pmc.ncbi.nlm.nih.gov/articles/PMC11614550/
本研究调查了 100 Hz 应用期间和之后 EA 刺激对单侧注射 6-羟基多巴胺 (6-OHDA) 创建的 PD 大鼠模型的影响。为了建立 EA 的最佳治疗参数,研究员们使用旷场和旋转测试动态评估运动行为。此外,他们还使用免疫电子显微镜评估了皮质纹状体脊柱的可塑性,并通过微透析、体内电化学和高效液相色谱法测量了多巴胺能和谷氨酸能神经递质的水平。

本研究通过使用Cerebus在体多通道神经信号采集系统(Blackrock Mircosystems)采集了运动皮层和纹状体中的局部场电位来记录神经活动动力学。此外,还采用化学遗传学技术来探测皮质纹状体谷氨酸能神经元,并阐明在 PD 大鼠模型中导致 EA 治疗益处的机制。
为了检查 EA 对运动症状的影响,研究员们最初评估了 PD 大鼠模型中的运动障碍。2 周后,由 6-OHDA 诱导病变的大鼠在旋转试验中表现出运动、行进距离更短和性能受损,表现出明显的运动障碍。接下来,研究员们研究了不同频率的 EA 刺激对 6-OHDA 损伤大鼠的影响。

图1:电针 (EA) 刺激动态缓解帕金森病大鼠模型中的运动缺陷,
而不影响黑质纹状体多巴胺功能障碍。
而不影响黑质纹状体多巴胺功能障碍。
由于纹状体不仅接受黑质纹状体 DA能投射,还接受皮质纹状体和丘脑纹状体谷氨酸能输入,研究员们评估了 EA 治疗对 DA 耗竭后谷氨酸能投射的影响。为了实现这一目标,他们首先评估了 vGluT1 和 vGluT2 的密度,它们作为投射到纹状体的皮质和丘脑谷氨酸能轴突末端的标志物。

图2:电针 (EA) 刺激有效调节皮质纹状体脊柱可塑性并减轻帕金森病大鼠模型中异常的谷氨酸传递。
为了进一步评估 EA 刺激的动态治疗效果,研究员们在运动皮层和背外侧纹状体中使用长期植入的电极进行了同步记录。观察到DA 耗竭导致在纹状体和运动皮层中观察到的高β振荡幅度显著升高。皮质纹状体相干性在高β范围内也有所增加。

图3:电针 (EA) 干预动态调节帕金森病大鼠模型中的病理性皮质纹状体 β 振荡同步。
为了实现对抑制皮质纹状体神经元的选择性抑制,研究员们在 6-OHDA 损伤大鼠中使用了由设计药物 (DREADD) hM4Di 独家激活的抑制性设计受体。进行αCaMKII 和 hM4Di-mCherry 标记的免疫染色以验证细胞特异性。

图4:皮质纹状体谷氨酸能神经元的失活减轻了具有 6-羟基多巴胺 (6-OHDA) 病变的大鼠的运动症状和高 β 振荡。
为了进一步阐明皮质纹状体谷氨酸能传递对 6-OHDA 病变大鼠 EA 治疗效果的贡献,研究员们试图通过长期施用 CNO 激活 hM3Dq-DREADD 来抵消 EA 的影响。

图5:在 6-羟基多巴胺 (6-OHDA) 引起病变的大鼠中皮质纹状体神经元的慢性激活中逆转电针 (EA) 效应。
越来越多的证据表明,EA 刺激通过多种方法对多巴胺能神经元提供神经保护作用。这些作用包括抗神经炎症、抗氧化应激和抗凋亡反应,以及调节肠道微生物组。

图6:左图说明了 EA 干预通过各种机制对多巴胺能神经元的神经保护作用,右图显示了结果表明,在 PD 大鼠模型中,EA 通过抑制过度的皮质纹状体谷氨酸传递来减轻运动缺陷和同步 β 振荡。
总之,本文的研究阐明了 PD 中 EA 治疗的时间动力学和最佳参数,它强调了抑制皮质纹状体谷氨酸传递在 EA 对 PD 的治疗益处中的重要性。
笔名:Liushuai
原文链接:https://pmc.ncbi.nlm.nih.gov/articles/PMC11614550/





