文献速递:一种快速的PROTAC新药筛选方法及在乳腺癌治疗中的应用
雌激素受体ERα的降解是治疗乳腺癌的一种有效策略。然而,耐药性问题限制了其效用,因此有必要开发下一代ERα靶向治疗方法。双特异性降解物(PROTAC)由于可同时结合靶蛋白(POI)和E3连接酶,高效催化靶蛋白的泛素化降解,近年来已成为一项很有前途的药物开发新策略。靶标结合配体的设计是PROTAC开发十分重要的环节。DNA编码化合物文库(DECL)筛选可能是鉴定此类新型配体的最佳选择。
在此背景下,美国X-Chem公司在Journal of Medical Chemistry发表了题为Bispecific Estrogen Receptor α Degraders Incorporating Novel Binders Identified Using DNA-Encoded Chemical Library Screening的文章。作者报告了一种新的ERα结合物和拮抗剂筛选流程:通过靶向ERα WT(野生型)和3个功能获得(GOF)突变体,基于DECL技术筛选了约1200亿个DNA编码分子,实现以最少的优化发现一系列新的ERα双特异性降解物(PROTACs)。

1 DNA编码化合物文库的亲和筛选
作者首先对1200亿的DNA化合物文库进行亲和筛选。将44种不同的DNA编码化合物文库组合,分别与无目标物、ERα WT配体结合域LBD(浓度7.7 μM-24 nM)、ERα WT(7.7 μM,含雌二醇15 μM)以及每种ERα突变体D538G、S463P和Y537S(均为7.7 μM)进行孵育。经一系列捕获、洗涤、洗脱、富集后进行测序。在所有44个文库中,共计产生5.28亿个单端reads,每个文库每种选择条件下的平均reads为120万个。
2 选择输出数据及Hit ID
将各个序列reads翻译成对应的构建单元,随后计算各选择条件下、每个库中所有构建单元组合的的富集概况以及各个构建单元组合共同富集的程度。如图2a,b显示,作者找到两个独立的构建单元对(双合成子),用作系列建立的起点化合物或hits。其在7.7和1.6μM ERα条件下均显著富集、与雌二醇竞争,且对Y537S和S463P突变体也有显著富集,可见其在配体结合位点结合。
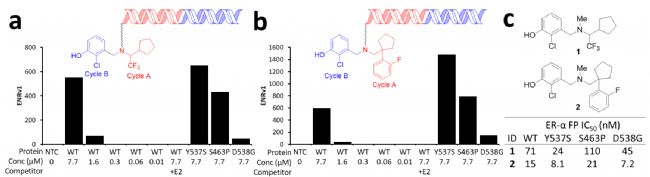
图2.(a,b)两个代表性构建单元结构及其富集示意图(c)两个最具效力的off-DNA化合物结构及其荧光偏振结合位移测定
3 Hit验证及其SAR研究
未验证输出选择,进行代表性off-DNA化合物的合成,并通过体外生物化学FP(荧光偏振)、对ER+细胞系MCF7在拮抗和激动模式下的增殖测定,以及在MCF7细胞中对PROTACs进行In-cell Western的ERα降解测定(Sapphire激光扫描成像系统,Azure Biosystems),鉴定出上述两个构建单元对的两个最具效力的代表性off-DNA化合物(1和2),如图2c所示。
在DECL筛选数据和分子对接的指导下,作者设计、制备并评估了体外小分子的结构活性关系(SAR),将其中具有显著强效拮抗作用,且未观察到细胞激动作用的化合物7作为双特异性PROTAC的一部分进一步改造。
4 ERα强效结合PROTAC的结合物开发
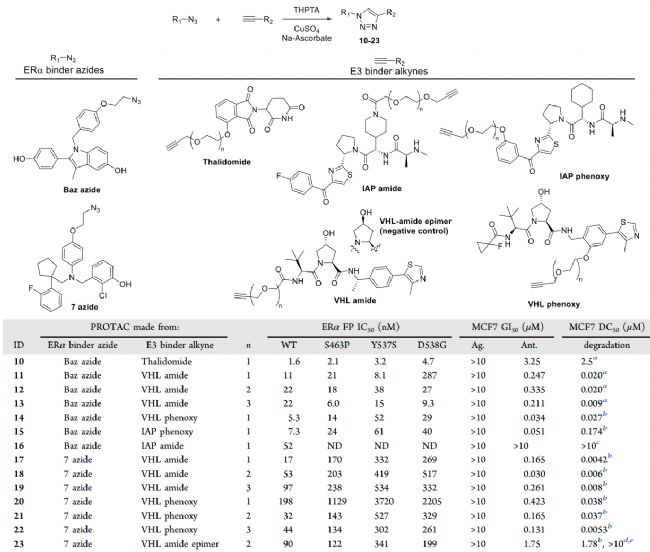
作者利用已知的ERα结合剂巴多昔芬,探索不同E3配体和连接体长度对ERα结合降解的影响。基于化合物7,1,3-偶极环加成制备了7种基于沙利度胺的化合物,结合实验中均为有效,其中11-14具有亚微摩尔细胞降解 (表2)。更进一步,基于VHL配体,设计制备了具有三个连接长度的PROTACs阵列。
表2. 利用巴多昔芬或化合物7组成部分作为POI配体的PROTACs
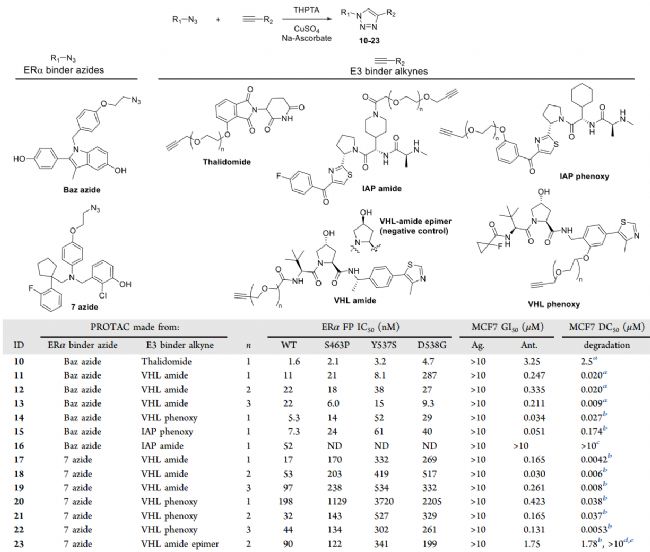
a原始分析. b48 h. c24 h. d6 h. e16 h.
5 ERα抑制降解的作用机制及动力学研究
对于其中最有效的两个VHL变体(18和21)的PROTACs,在MCF7细胞中进行In-cell Western降解试验(Sapphire激光扫描成像系统,Azure Biosystems),结果显示在24 h时,两种化合物的ERα水平呈剂量依赖性降低,21的降解能力强于18(补充图S2)。MCF7细胞活力测定显示,激动剂作用可忽略不计,而两种化合物都显示出强大的拮抗活性。
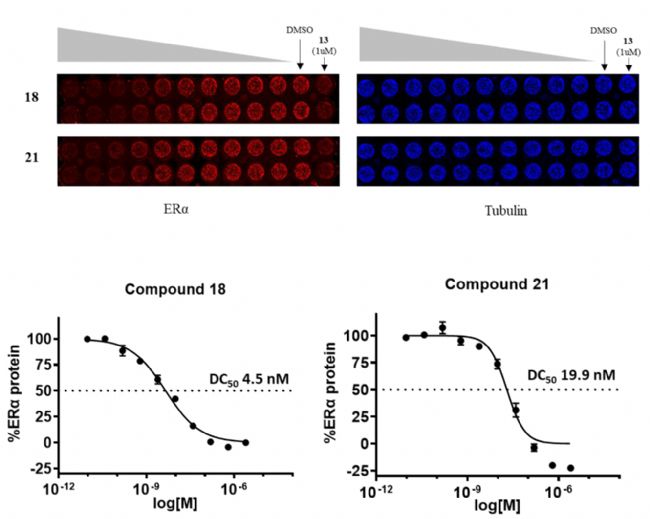
图S2. PROTACs在MCF7细胞中抑制并降解Erα。In-cell western 实验(Sapphire激光扫描成像仪拍摄)中的化合物18和21剂量反应曲线
为评估PROTAC介导的ERα降解动力学,作者在时程实验后进行Western Blot(Sapphire激光扫描成像系统,Azure Biosystems)。结果显示, PROTAC的降解剂18效果早在2小时就可看到强烈的、近乎完全的降解(图4a),显著优于富维司汀(4小时后出现降解,无完全降解)。E3结合剂VHL-298竞争实验(图4c) ,以及阴性对照(18的VHL脯氨醇差向异构体23)实验均证明,蛋白酶介导的ERα降解需要vhl参与(图4c) 。
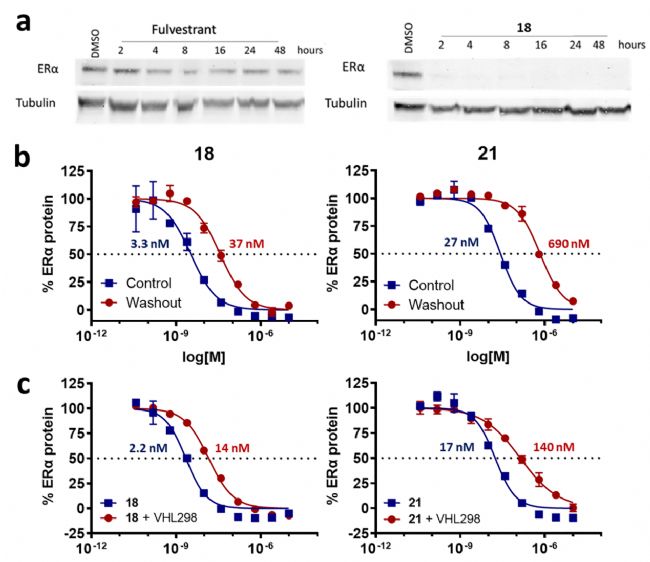
图4. 富维司汀及PROTACs 18、21在MCF7细胞中抑制和降解ERα。
在另一种ER阳性细胞系T47D中Western Blot(Sapphire激光扫描成像系统,Azure Biosystems),测试ERα PROTACs 18和21。结果与MCF7细胞系相似,在T47D细胞中观察到明显的ERα降解 (图5a)。作者随后用剂量递增的ERα PROTACs 18和21处理各类乳腺癌细胞系7天。结果显示所有ER+细胞系均存在活力缺陷,而ER阴性MBA-MB 231和永生化的乳腺细胞系MCF10A未见有活力影响(图5b)。证实了这一新型ERα PROTACs系列的在靶(on target)效应。
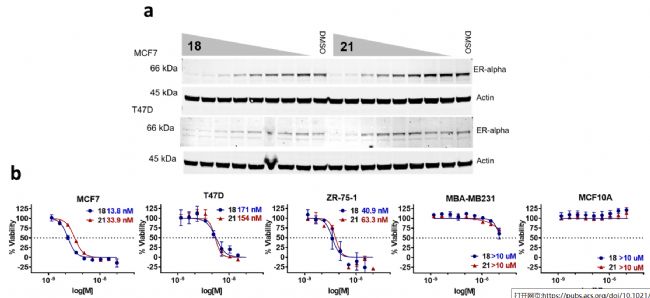
图5. (a) 18和21在MCF7和T47D细胞系的ERα降解(b)ERα PROTACs在各类乳腺癌细胞系中的在靶作用
6 体外ADME和PK
总体而言,基于VHL的酰胺和苯氧基化合物17-22是ER+细胞系中ERα的有效降解剂。选择连接链较短的化合物17、18、20和21进一步研究(表3)。在体内,VHL苯氧基化合物20和21的静脉注射清除率远低于VHL酰胺17和18,且前者分布体积也远低于后者,故20、21的暴露量高于17、18。口服给药18和21时观察到的暴露量最小,但仍表现出强大的降解活性和显著的血浆暴露,且在皮下给药时具有不同的PK特征,因此值得在体内评估ERα的降解情况。
表3. 雄性CD1小鼠中选定化合物的体外清除率和体内药代动力学(PK)
7 体内疗效研究
化合物21皮下注射10 mg/kg也具有显著的肿瘤生长抑制效果,TGI= 84.3%,p < 0.001。化合物18对肿瘤体积的影响较小,因此在第20天停止给药(图6a)。终点PK分析显示,血浆和肿瘤中的暴露与体内观察到的疗效密切相关,化合物21的暴露量远高于18(图6c,d)。Western Blot结果表明(Sapphire激光扫描成像系统,Azure Biosystems),所有治疗组的ERα水平均有所降低(图6e)。这些结果清楚地表明,化合物21是在体内外抑制和降解ERα的优秀工具化合物。
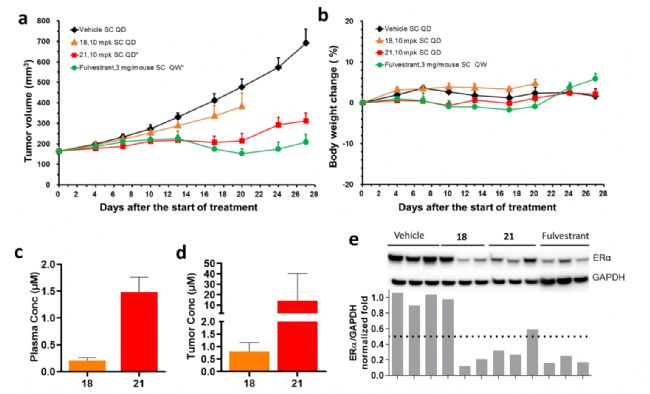
图6. 体内疗效和PK/PD研究表明MCF7异种移植模型有效。(a) 18、21与富维司汀的抗肿瘤活性对比。(b)所有化合物耐受性良好,体重无变化。(c, d) 末次给药3 h 后18和21的终末血浆PK和肿瘤PK (e) Western blot(Sapphire激光扫描系统拍摄)显示18、21及富维司汀治疗后的ERα水平降低。
8 总结
DNA编码化合物文库(DECL)作为设计PROTACs的筛选平台具有显著优势。基于此,本文设计、优化、制备了一组有效的Erα双特异性降解物,是进一步开发基于ERα的PROTACs乳腺癌治疗药物的价值工具。
原文链接:
https://pubs.acs.org/doi/abs/10.1021/acs.jmedchem.1c00127





