CERO全自动细胞培养仪在生物医学研究突破性进展中的应用文献汇总
为什么选择CERO 3D培养系统?
高精度:可持续监测和控制温度、pH值及二氧化碳等关键参数。
可扩展性:最多可同时管理4个独立控制的CEROtubes,每个管体容量可达50毫升。
可重复性:标准化流程确保每次使用都能获得一致的高质量结果。
降低剪切应力:温和的搅拌和培养环境保护细胞,提升其生长和存活率。
无需耗材:无需基质胶(避免外源物质)、无需支架的3D培养(避免昂贵耗材)。
生成同基因异质ACVRL1(wt/mut)敲除iPS细胞系,用于HHT2相关血管生成的体外研究
在这项研究中,使用了CERO 3D孵化器和生物反应器系统来孵育和培养iPSCs,在形成胚胎体(EBs)过程中进行培养,并在内皮分化过程中进行持续培养。该研究描述了通过CRISPR/Cas9介导的ACVRL1基因敲除,在诱导多能干细胞(iPSCs)中建立体外血管生成疾病模型,以研究HHT2疾病中的血管生成障碍。研究者在ACVRL1基因中创建了一个异质的17个碱基对框移突变,反映了HHT2患者的血管生成疾病特征。iPSCs的内皮分化通过免疫细胞化学法进行了监测。151个与TGF-beta/BMP相关的基因表达分析通过RT-qPCR进行了评估。
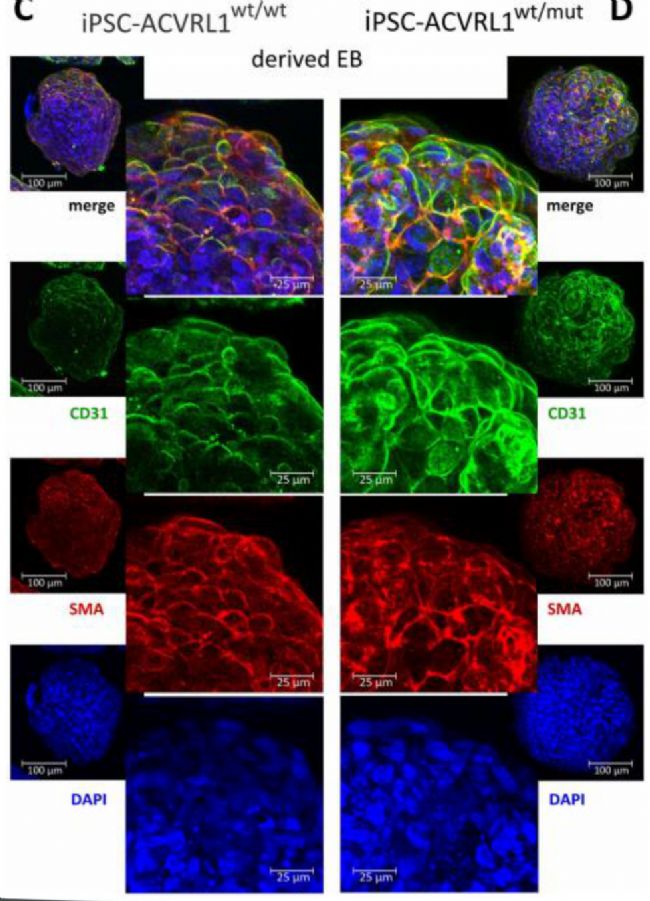
”胚胎体(EBs)中内皮分化的诱导。图示为共聚焦显微镜图像,展示了(A)ACVRL1wt/wt和(B)ACVRL1wt/mut胚胎体在内皮诱导后CD31+细胞的出现。使用Phalloidin标记F(丝状)-肌动蛋白细胞骨架,DAPI用于染色细胞核。(C,D)使用抗平滑肌肌动蛋白的抗体对胚胎体进行染色,以检测可能的周细胞结构。”
作者:Xiang-Tischhauser 等人(2023)
期刊: Cells
出版日期: 2023年6月
卷号: 12(12)
文章编号: 1600
利用台式生物反应器平台在完全定义条件下标准化生成来源于人类iPSC的造血类器官和巨噬细胞
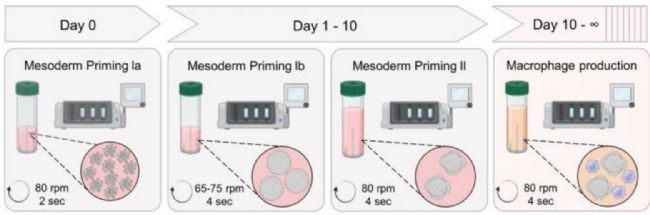
在这项研究中,使用CERO3D孵化器和生物反应器生成3D造血类器官,以生产iPSC衍生的巨噬细胞。研究提出了一种新方法,利用无外源动物成分和化学定义的生物反应器平台生产免疫细胞。文章特别聚焦于从来源于诱导多能干细胞(iPSCs)的3D造血类器官中持续生成具有功能性和表型相关的巨噬细胞(iPSC-Mac)。研究人员展示了从三种不同的分化iPSC系中高效且持续地产生巨噬细胞的能力,且所生产的巨噬细胞具有一致且可重复的表型和功能特征。所生成的iPSC-Mac可以作为测试免疫调节药物的模型。
作者:Ackermann 等人(2024)
期刊: Stem Cell Research & Therapy
出版年份: 2024
卷号: 15
文章编号: 171
可扩展生成功能性人类iPSC衍生的CAR-巨噬细胞,有效清除CD19阳性白血病
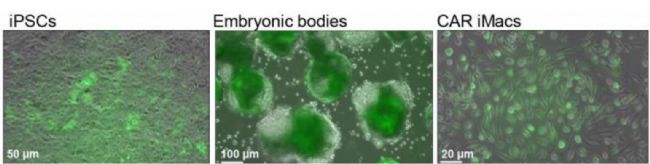
在这项研究中,使用CERO生物反应器进行CAR-iMacs的持续扩增生产。研究重点展示了造血类器官的形成,这些器官持续释放CAR-iMacs。研究者在不同的时间点从正在进行的生物反应器分化过程中收获了CAR-iMacs,这些细胞来自上清液。
本文提供了使用现代扩增技术从不同干细胞来源生成CAR-巨噬细胞的结果,这些技术用于下一代免疫细胞培养。生成的细胞表现出增强的功能,包括增强的抗原依赖性吞噬作用,能够吞噬CD19+目标癌细胞,同时伴有增强的促炎反应。
作者:M. Abdin 等人(2023)
期刊: Journal for Immunotherapy of Cancer
出版年份: 2023
卷号: 11(12)
文章编号: e007705
生成同基因异质合成ACVRL1(wt/mut)基因敲除iPS细胞系,用于HHT2相关血管生成的体外研究
本研究中,CERO3D培养箱和生物反应器与海藻酸盐微载体结合用于hPBMCs的培养。
本文报道了人外周血单核细胞(hPBMCs)在体外促炎状态下的研究。文章旨在调查在应对疾病或阿尔茨海默病特异性细胞毒分子时,细胞因子的释放变化。研究观察了TNFa和p40的细胞内含量。
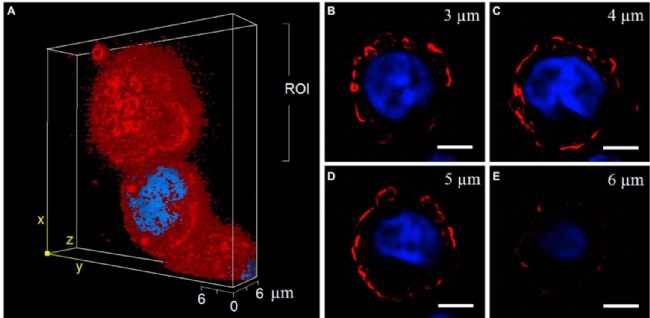
蓝色:DNA+DAPI
红色:rAβ42+CRANAD-2
“激光扫描共聚焦显微镜下,悬浮hPBMCs(n = 50,1n = 单个分析细胞)在与rAβ42(15 nM)孵育24小时后的代表性3D影像(A)。数据集由感兴趣区域(ROI,x–z平面)中4个光学切片组装而成,步长为1 μm(B–E)。蓝色 – 核DNA由DAPI染料染色;红色 – rAβ42由CRANAD-2染色。标尺 = 5 μm。”
作者:Kot等人
期刊:Front. Neurosci.
卷号:第18卷
出版年份:2024
溶血磷脂酸通过诱导自噬活性抑制高级别浆液性卵巢癌细胞的凋亡,并通过EGFR-PI3K/AuroraAThr288-geminin双重信号通路促进细胞周期进展
在本研究中,CERO 3D 培养箱和生物反应器用于培养A2780细胞和OVCAR5类胚体悬浮培养。
研究人员显示,溶血磷脂酸(LPA)可以通过诱导自噬活性抑制高级别浆液性卵巢癌细胞的凋亡,并通过EGFR-PI3K/Aurora-AThr288-geminin双重信号通路促进细胞周期进展。
该研究为增强HGSOC精准医学的临床效益提供了潜在靶点。

作者:Zhao等人
期刊:Front Pharmacol.
卷号:第13卷
文章编号:1046269
出版年份:2022
面向应用的人类iPSCs在冷冻袋中的大宗冷冻保存,随后直接接种于可扩展悬浮生物反应器中进行扩增和神经分化
在本研究中,CERO 3D 培养箱和生物反应器用于不同人类iPSC系的培养及其神经分化。
本文展示了对人类iPSC系UKKi011-A和BIONi010-C-41的大宗冷冻保存研究,这些干细胞在再生医学中具有潜在的应用。文章讨论了用于大宗冷冻保存的方法,以及冷冻细胞解冻后接种到可扩展悬浮生物反应器中进行扩增和神经分化的结果,最后得出结论,认为该技术有助于避免前期培养,从而实现时间和成本效益高的治疗方法,且能处理大量细胞。

“UKKi011-A和BIONi010-C-41细胞在接种到可扩展生物反应器前后的形态学变化。(A)工作流程的简化示意图。hiPSC系UKKi011-A和BIONi010-C-41采用慢速冷冻法在冷冻管(1 mL,总计2 × 10⁷细胞)和冷冻袋(50 mL,总计1 × 10⁹细胞)中以2 × 10⁷细胞/mL的密度进行冷冻保存,并在解冻后直接接种到CERO 3D悬浮生物反应器中(= 干性维持)。(B)相差显微镜图像显示了两种细胞系在冷冻保存前的2D形态学。标尺表示200 μm。(C)代表性相差显微镜图像,展示了UKKi011-A类胚体在悬浮生物反应器中第1天和第3天的形态变化。对于非冷冻样本,展示了冷冻管和冷冻袋中冷冻保存样本解冻后的第1天和第3天的形态学变化。标尺表示500 μm。”
作者:Meiser等人
期刊:Cells
出版日期:2023年7月
卷号:第12卷
期号:第14期
重现神经外胚层暴露的造血祖细胞,实现在大规模生产可冷冻保存的iPSC衍生人类小胶质细胞
在本研究中,CERO 3D 培养箱和生物反应器用于大规模生产来自人类iPSC的胚胎体,并且共培养含有iPSC衍生小胶质细胞(iPSdMiG)的皮层类胚体培养物,培养周期为1至4周。
该研究提供了利用诱导多能干细胞(iPSCs)生产人类小胶质细胞的信息,后者是中枢神经系统的固有免疫细胞。本文展示了一种大规模生产和冷冻保存iPSC衍生小胶质细胞(iPSdMiG)的体外分化方法,这些小胶质细胞具有与成人人类小胶质细胞高度相似的转录组特征,且对典型小胶质细胞标志物呈免疫阳性,能够分泌促炎细胞因子,参与吞噬活性,产生反应性氧种,并且适用于神经2D和3D系统中的共培养研究。
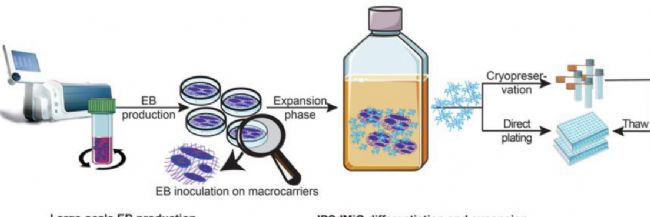
大规模胚胎体(EB)生产 iPSdMiG分化与扩增
“示意图展示了通过大规模生产胚胎体(EB)生成iPSdMiG的过程,这些胚胎体既表现出原始造血作用,又包含早期神经前体,并随后在网状宏载体上进行扩增。小胶质细胞可以从第6周到第12周的分化过程中持续收获。”
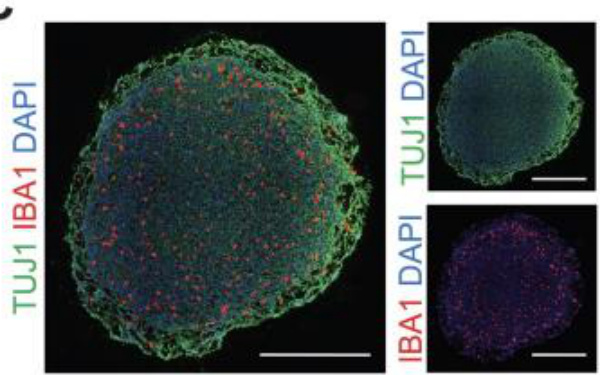
“C 代表性免疫荧光图像显示,iPSdMiG(IBA1,红色)迁移到并均匀分布在3D皮层类胚体中(TUBB3,绿色);细胞核用DAPI染色。标尺=500 μm。
D 高倍放大图像揭示,集成的iPSdMiG(IBA1,红色)在与3D皮层类胚体(TUBB3,绿色)共培养4周后表现出分支形态。标尺=100 μm。”
作者:Mathews等人
期刊:Stem Cell Reviews and Reports
出版年份:2022
iPSC及其衍生物在多个谱系中的可扩展扩增
本文讨论了诱导多能干细胞(iPSCs)在各种生物医学应用中的使用,特别是用于毒性测试。作者描述了使用CERO 3D悬浮培养平台和台式生物反应器进行iPSCs可扩展生产的策略。文章还报告了最近的工作,旨在建立稳健的可扩展分化方案,涉及心脏、神经和肝脏命运,以增加可用的研究工具。
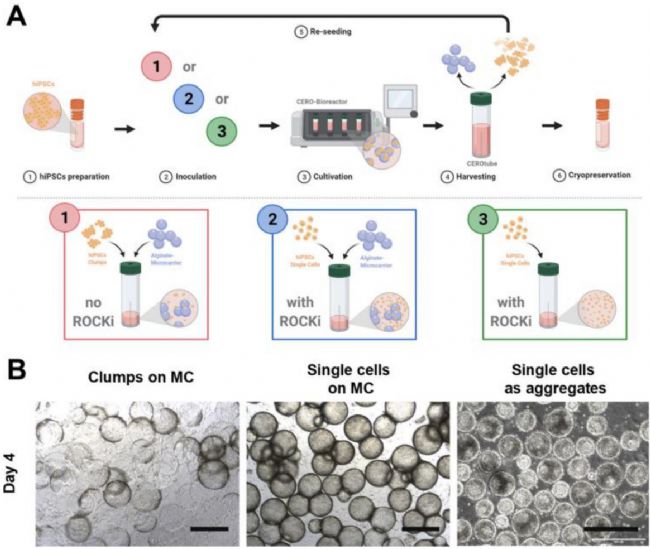
在3D培养条件下培养和扩增iPSCs。
A:3D悬浮培养的工作流程选项。
A1:iPSC团块被接种在Matrigel涂层的海藻酸盐微载体上。
A2:iPSC单细胞被接种在Matrigel涂层的海藻酸盐微载体上,培养基中添加了10 μM Y-27632。
A3:iPSC单细胞悬液在ROCK抑制剂Y-27632的支持下形成聚集体。
B:作为团块和单细胞在Matrigel涂层的海藻酸盐微载体(MC)和聚集体上的细胞形态。细胞系UKBi005-A用于微载体方法,细胞系BIONi010-C用于聚集体方法。标尺=500 μm。
作者:Keong Kwok等人
期刊:Reprod Toxicol.
出版日期:2022年5月17日
文章编号:S0890-6238(22)00068-5
人类iPSC衍生肝细胞在2D和3D悬浮培养中的冷冻保存与体外毒性研究
本文讨论了诱导多能干细胞(iPSCs)在各种生物医学应用中的使用,特别是用于毒性测试。作者描述了使用CERO 3D悬浮培养平台和台式生物反应器进行iPSCs可扩展生产的策略。文章还报告了最近的工作,旨在建立稳健的分化方案,涉及将iPSCs分化为肝细胞,并通过生物反应器平台进行大规模培养。这些工作有助于提升iPSCs在毒性测试等应用中的潜力。
作者:Altmaier等人
期刊:Reproductive Toxicology
卷号:第111卷
出版日期:2022年8月
页码:68-80页
人类多能干细胞在动态培养系统中功能性分化及可扩展生产肾脏近端小管上皮细胞
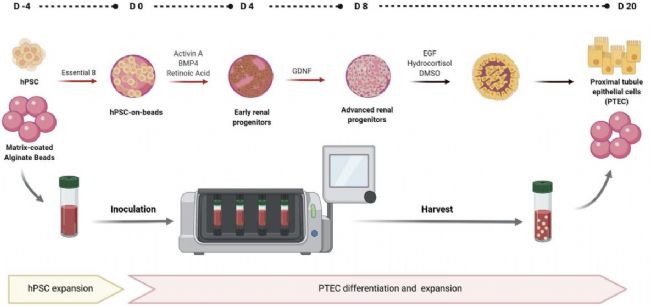
本文介绍了一种大规模生产人类多能干细胞(hPSC)衍生的肾脏近端小管上皮细胞(PTEC)的方案。研究人员成功地在悬浮生物反应器中扩增hPSC,并使用CERO 3D培养箱(前身为BioLevitator)在基质涂层的海藻酸盐珠上将其分化为PTEC。文章解释了PTEC在血液清除、体内稳态维持、废物排除和前尿中物质的主动重吸收中具有重要作用。PTEC可用于模拟药物引起的肾毒性。
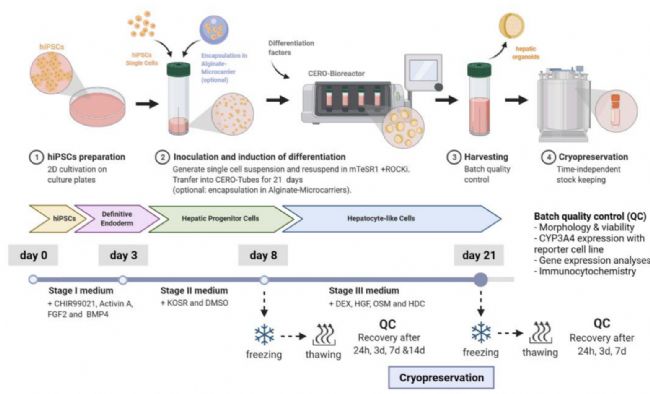
“人类iPSC衍生肝细胞在悬浮培养(3D)中的分化流程概述。第一步是建立稳健的2D分化方案,将肝细胞(HLCs)从初始阶段分化至成熟阶段。第二步,将该方案转化为CERO 3D(OLS)悬浮生物反应器中的3D培养模式。最后,在两个分化时间点(第8天和第21天)对肝脏类器官进行冷冻保存,以评估存储效率。分化过程中和解冻后的恢复过程中进行的不同质量控制(QC)展示了肝脏类器官的质量。”
作者:Ngo等人
期刊:Cell Prolif.
出版日期:2022年3月
卷号:第55卷
期号:第3期
文章编号:e13190
人类iPSC衍生肝细胞在2D和3D悬浮培养中的冷冻保存与体外毒性研究
在本研究中,CERO 3D培养箱和生物反应器用于无支架的肌球体形成和扩增。
本研究讨论了使用中型培养箱和生物反应器混合系统生产无支架的肌源性类球体。文章比较了来自初代猪肌肉细胞的类球体与来自C2C12细胞系的类球体,观察并比较了它们的形态、增长参数、标志物表达和肌源性潜力。

“悬浮培养中的肌球体形成。C2C12(a)和猪初级肌肉细胞(PMCs,(b))分别以200,000或100,000个细胞/mL的密度接种到CERO 3D培养箱和生物反应器(OLS)中,并对7天内的肌球体形成进行分析。在所有时间点均观察到大量圆形肌球体。底部图像(右侧)显示了第4天肌球体的放大图。标尺:200 μm。”
作者:Stange等人
期刊:Cells
出版日期:2022年5月
卷号:第11卷
期号:第9期
文章编号:1453
用于高效体外研究纳米颗粒配方的微流控3D肠道肿瘤类胚体模型
在本研究中,使用CERO 3D培养箱和生物反应器生成来自人类结肠癌细胞系HT29-MTX-E12的肿瘤类胚体。
本文提供了一个微流控3D肠道肿瘤类胚体模型的开发信息,该模型允许测试功能化纳米颗粒及其通过粘液层的渗透。引言指出口服给药是首选方式,口服药物的有效性依赖于生物利用度。
纳米颗粒是改善医疗治疗的重要工具,因此,可以通过体外测试来评估纳米颗粒药物传递系统的靶向输送和效果。
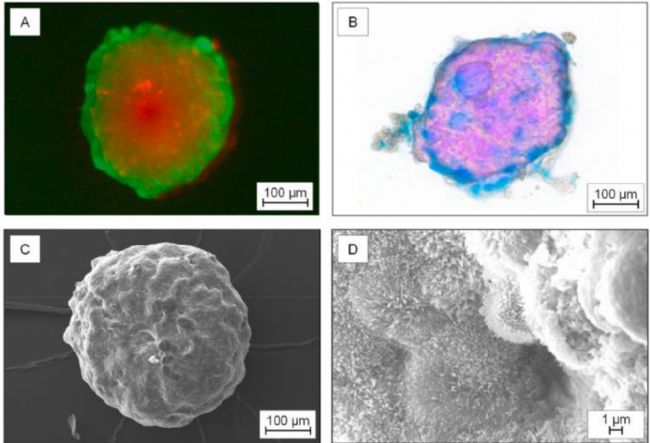
“生成的HT29-MTX-E12细胞系3D肿瘤类胚体的表征
A) 活死细胞染色:使用荧光染色法同时标记存活细胞(calcein-AM,绿色)和死亡细胞(碘化丙啶(PI),红色)。
B) 组织学染色的类胚体:核快速红 – 细胞核;Alcian蓝 – 酸性黏多糖和醋酸黏蛋白。
C) 类胚体的扫描电镜图像;
D) 扫描电镜图显示表面微绒毛。”
作者:Elberskirch等人
期刊:Journal of Drug Delivery Science and Technology
卷号:第63卷
出版日期:2021年
文章编号:102496





