使用Emulate人肺气道器官芯片建立肺囊性纤维化模型
肺囊性纤维化(pulmonary cystic fibrosis,PCF)是一种遗传性疾病,由编码囊性纤维化跨膜传导调节因子的基因突变引起,会产生气道粘膜纤毛清除受损、肺炎以及呼吸功能障碍等症状。目前尚缺乏能够完全模拟PCF患病组织细胞特性的体外实验模型,而人肺气道器官芯片模型则很好地填补了这一空缺,这里我们对应用人肺气道芯片建立体外肺囊性纤维化模型的有效性进行总结。
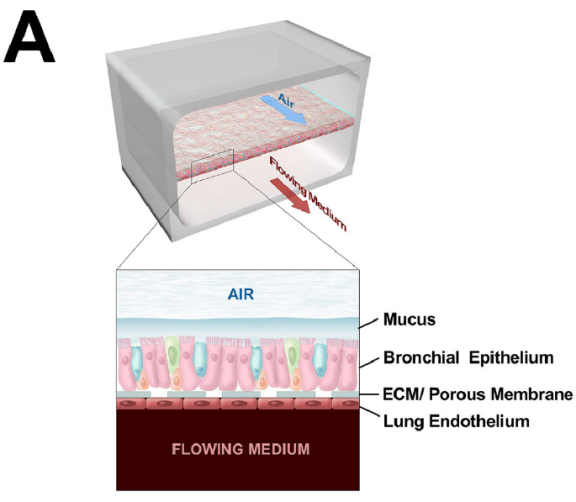
图1 人肺气道芯片结构示意图
一、患者组织来源的肺气道芯片再现PCF的病理学特征:
本研究分别使用健康人和PCF患者的原代支气管上皮细胞,构建了健康人和患者的肺气道芯片。通过对不同标志性蛋白(如ß-tubulin、CK5、CC10、Muc5AC等)的染色检测,可以看到上皮细胞特化为纤毛细胞、基底细胞、棒状细胞和杯状细胞;此外,PCF肺气道芯片上皮层表面纤毛细胞覆盖率明显高于健康上皮层,且表现出更高的纤毛跳动频率。同时,研究者对芯片通道中的收集液进行了Alcian蓝染色以定量粘蛋白丰度,结果表明CF肺气道芯片显示出更丰富的粘蛋白积累。以上结果共同表明,CF肺气道芯片再现了PCF患者气道上皮的组织学特征。
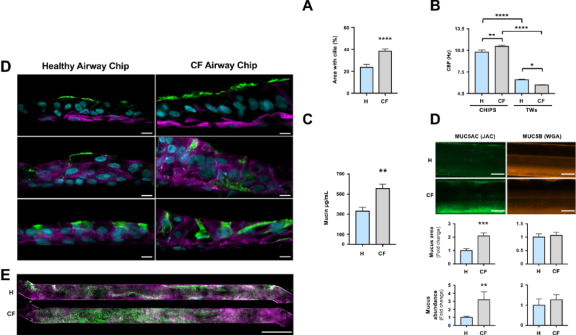
图2健康人芯片和PCF患者芯片的纤毛和粘蛋白比较
二、肺气道芯片再现PCF的炎症反应特征
接下来研究者观察PCF肺气道芯片的血管通道,发现与正常气道芯片相比,炎症因子含量IL-8显著增加;向芯片的血管通道中加入多形核白细胞,观察到与正常气道芯片相比,CF芯片中多形核白细胞向内皮细胞的粘附效应增强,与PCF患者肺部免疫细胞浸润增加的行为相似。这两个现象表明,PCF气道芯片能表现出与PCF相似的炎症反应特征。
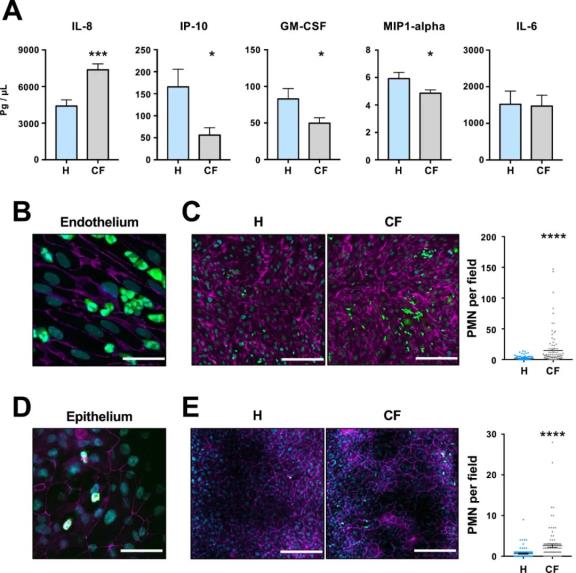
图3健康人与PCF患者气道芯片的炎症反应表型比较
三、绿脓杆菌感染可引起CF肺气道芯片产生与PCF相似的免疫炎症反应
研究者将GFP标记的绿脓杆菌接种于芯片中,以模拟绿脓杆菌肺部感染。荧光密度定量结果显示PCF芯片中的细菌数量更高、炎症细胞因子(如IL-6、TNF-α和GM-CSF)分泌增加、绿脓杆菌感染处有更多的多形核白细胞募集。这与临床上PCF患者肺部感染后炎症反应特征类似。以上结果共同说明,PCF芯片能真实再现PCF气道的结构和病理生理学特征尤其是炎症反应相关的特征。
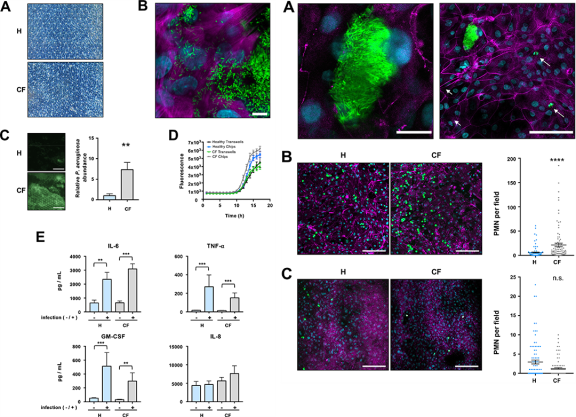
图4 绿脓杆菌感染下的健康人和PCF患者芯片比较
研究结论
利用Emulate器官芯片这一体外培养体系,研究人员成功构建了来源于患者的PCF气道芯片模型,该模型在体外表现出了与患者临床症状极为相似的病理学表征,在经细菌感染后,PCF芯片亦能够表现出与患者相似的病理特征,这说明人肺气道芯片能应用于建立PCF模型以及后续药物测试、机制探索等研究,有助于推进PCF发病机制和临床治疗手段的发展。
参考文献:
1. Plebani R. et al. Modeling pulmonary cystic fibrosis in a human lung airway-on-a-chip. J Cyst Fibros 21, 2022. doi:10.1016/j.jcf.2021.10.004.





