CRISPR-Cas9基因编辑类器官模型助力贲门向贲门癌早期转化研究
约翰霍普金斯大学Stephen J Meltzer于2022年11月30日发表在SCIENCE TRANSLATIONAL MEDICINE(19.319/Q1)上题为“Generation and multiomic profiling of a TP53/CDKN2A double-knockout gastroesophageal junction organoid model”的文章,TP53和CDKN2A的失活发生在贲门(GEJ)肿瘤发生早期,但前期缺少贲门向贲门癌转化的模型,本研究通过类器官和基因编辑相结合,在正常贲门类器官模型上,把TP53 / CDKN2A基因双敲除,模拟了癌症转化过程包括代谢和表观基因组等变化,为肿瘤研究及临床治疗缺少合适模型时,提供了新的思路。
研究项目背景:
TP53和CDKN2A的失活发生在贲门(GEJ)肿瘤发生早期。由于缺乏GEJ特异性疾病模型,尚未研究TP53和CDKN2A在GEJ失活的癌症促进影响。本研究通过野生型原代人GEJ类器官模型和CRISPR-Cas9介导的TP53和CDKN2A双敲除编辑的转化GEJ类器官模型。双基因敲除的GEJ类器官体外形态表现发育不良、具有原肿瘤特征以及能够小鼠体内成瘤。
脂质组学分析成功筛查到变化最显著的脂质—血小板活化因子(PTAF)。通过siRNA干扰或抑制剂(WEB2086)抑制PTAF/PTAF受体减弱了TP53 / CDKN2A基因敲除类器官的增殖和体内成瘤。TP53 / CDKN2A双重失活破坏了转录组和DNA甲基组,特别是FOXM1。FOXM1通过与PTAF受体启动子结合激活PTAFR转录,进一步扩增PTAF-PTAFR途径。
研究路线图
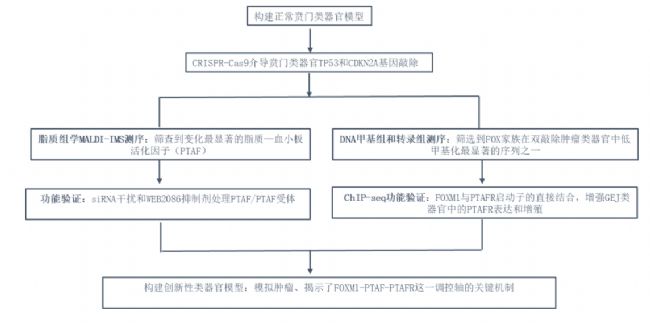
研究结果
1人正常贲门类器官的建立和表性特征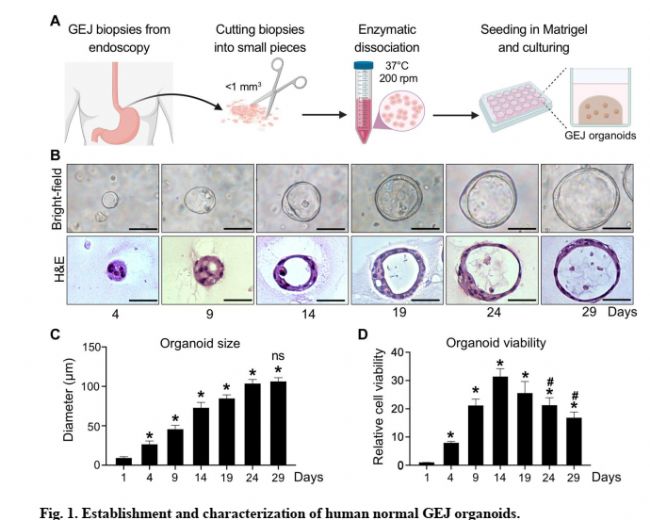
2 TP53/CDKN2A双基因敲除促进贲门类器官的增殖、增生和肿瘤转化
3 脂质组学MALDI-IMS 测序:在TP53/CDKN2AKO贲门类器中筛选到PTAF 变化最显著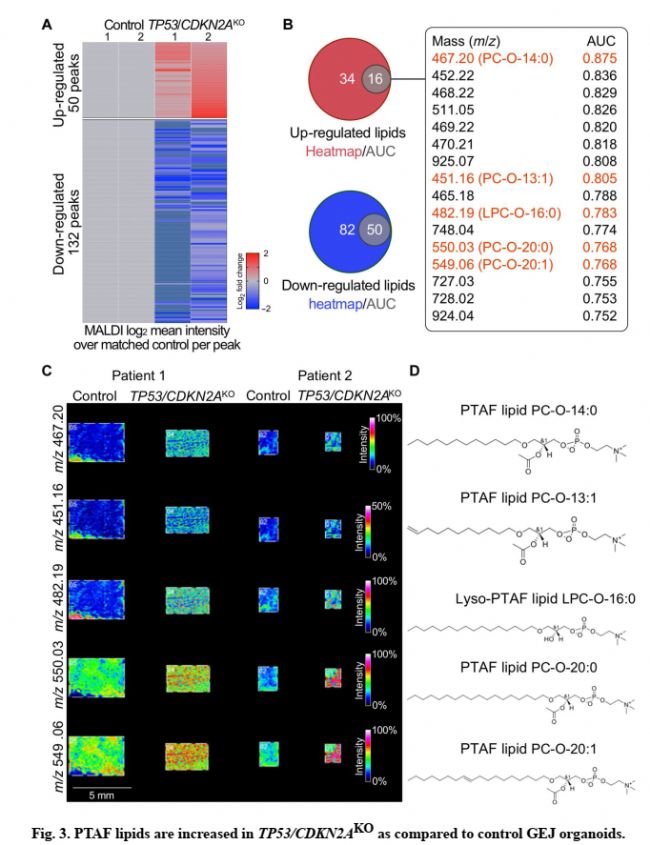
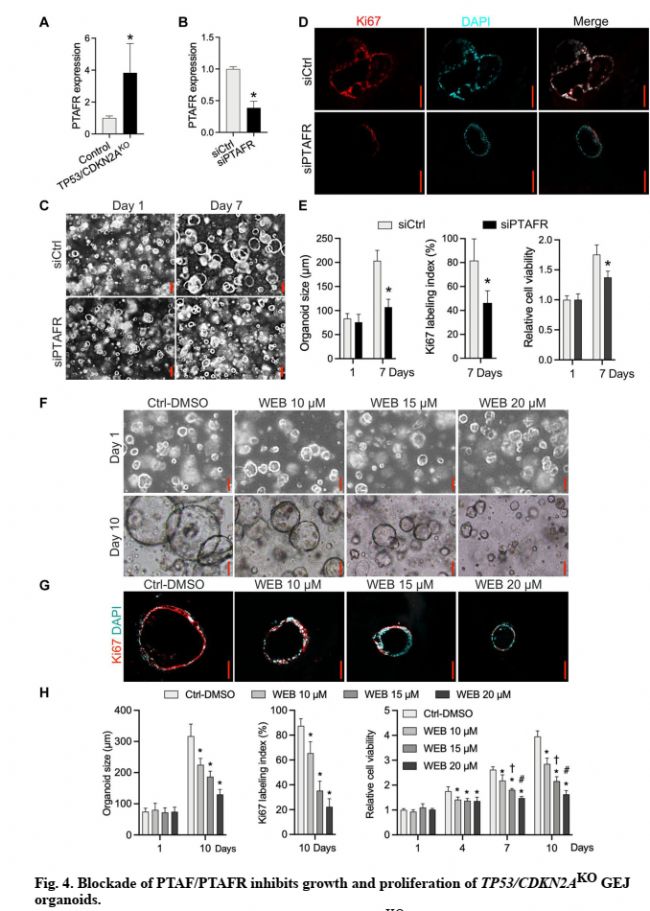
4 通过siRNA干扰和抑制剂WEB2086抑制PTAF/PTAF表达,达到抑制TP53/CDKN2AKO贲门类器官增值和小鼠体内成瘤
5 DNA甲基组和转录组测序:筛选到FOX家族在双敲除肿瘤类器官中低甲基化最显著的序列之一

6 ChIP-seq功能验证:FOXM1与PTAFR启动子的直接结合,增强GEJ类器官中的PTAFR表达和增殖
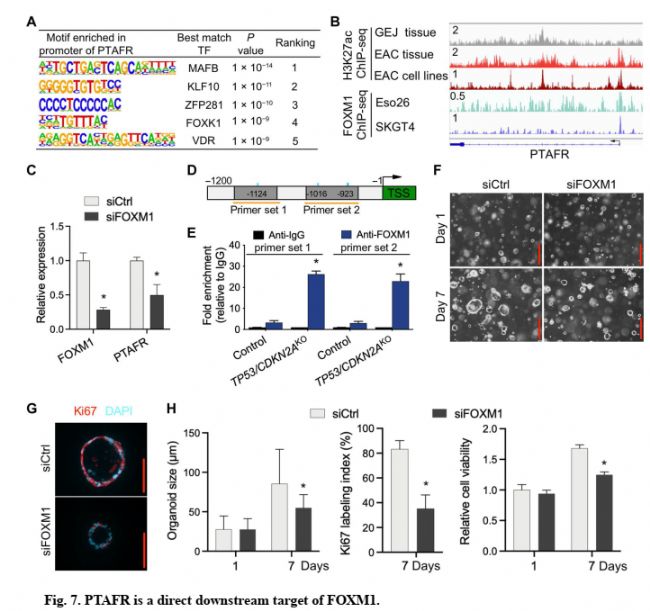
本研究中,通过基因编辑对两种关键的抑癌基因进行敲除,成功诱导贲门类器官向肿瘤方向转化,构建贲门-贲门癌转化类器官模型,为肿瘤早期发生发展的探索提供了新的方向,也为后续其他临床疾病研究提供了造模的新方向,造模的新方向—类器官模型。





