小鼠模型在血液病研究中的应用
血液生病了?小鼠模型助力细胞基因治疗,为血液病研究带来新希望
如果说骨骼是人体的行动支撑,那么血液,则是人体的动力之源。
一旦血液发生问题,对于人体而言,可谓是牵一发而动全身。
血液类遗传疾病通常比较复杂并且很难彻底治愈,会对身体造成巨大的伤害。例如地贫、镰状细胞贫血、血友病等等,患者往往自幼发病,无法大胆地运动,且需要终身治疗,为患者家庭和社会带来了很重的经济负担。
而细胞基因治疗,则为这类遗传疾病的彻底治愈带来了新的希望。从最初的基础研究阐明疾病的发病机制,到发现基因编辑新方法的可行性验证,再到细胞基因治疗的有效性评估等等方面,这些都离不开前期在小鼠模型中开展的临床前的体内实验结果。
今天,J博士就来给大家唠唠小鼠模型在血液疾病中的研究策略。
β地贫和SCD的基因治疗策略:
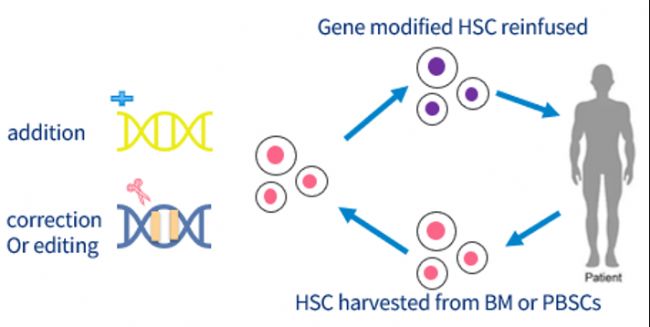
β地贫和SCD患者都是由于遗传到有缺陷的基因,导致β珠蛋白的功能缺陷,呈现不同严重程度的疾病表型。因此基因治疗策略往往有:
1)导入正常基因替代缺陷基因;
2)直接编辑纠正致病基因;
3)导入具有治疗性的基因。
Addition——Bluebird bio:
LentiGlobin (Zynteglo) Beti-cel; BB305
LentiGlobin (Zynteglo) Beti-cel; BB305
2022年8月17日,全球首个治疗输血依赖型β地贫的细胞基因疗法beti-cel获FDA批准上市,此前该疗法已于2019年获EMA批准。
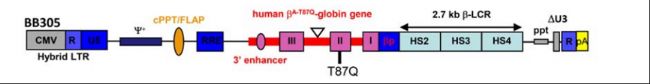
在自体造血干细胞中稳定引入正常的β珠蛋白基因可以规避同种异体细胞移植的局限性和风险,从而有效治疗β珠蛋白缺陷相关的疾病。如蓝鸟公司的beti-cel中采用的BB305载体,其构建如下图:
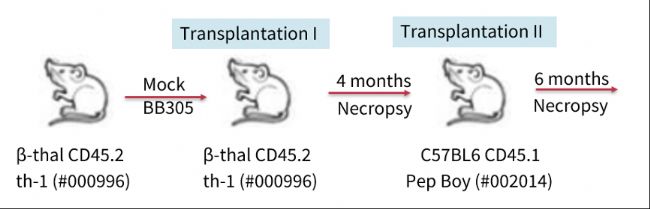
01 实验设计与小鼠模型
02 药效评估
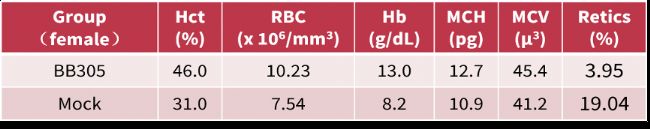
在第一代移植后4个月,实验表明自体移植的细胞可长期存活,且βA-T87Q-珠蛋白可持续生成,此外小鼠红细胞参数分析显示贫血表型得到改善,具有治疗效果。血液生化学数据也表明未出现与βA-T87Q-转基因蛋白生成相关的毒性。
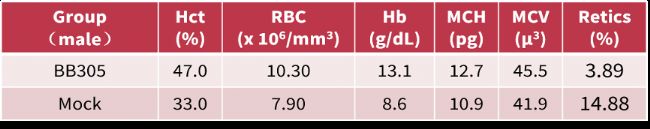
03 安全性评估
为了深入了解插入诱变对恶性肿瘤(白血病)生成的潜在影响,以评估长期安全性,该研究中进行了涉及108个B6 CD45.1小鼠(Pep boy #002014)的二次移植。除了常规分析了移植中的载体拷贝数以及插入位点情况外,还用CD45.1和CD45.2的抗体,确定增殖性病变的起源是继发性还是非继发性受体起源。此外因为该实验中需要用辐照清髓来降低排斥反应,所以部分肿瘤的发生有可能与辐照还有小鼠的遗传背景有关,因此,该药物也在免疫缺陷鼠NOD/SCID (#001303)中做了安全性测试,结果表明没有与BB305相关的毒性或致瘤性[1]。
Correction——
BEAM Therapeutics: BEAM-102
BEAM Therapeutics: BEAM-102
碱基编辑也是目前基因疗法中的热门。其可以在不导致DNA双链断裂的情况下,实现基因组中的单个碱基精确修改,如腺嘌呤碱基编辑器(ABE),能够将A转换为G。
像BEAM Therapeutics的BEAM-102就采用了该策略来治疗SCD。在SCD中,该ABE方法虽然不能还原突变,但是产生的珠蛋白变体不具有致病性,原理如下图:
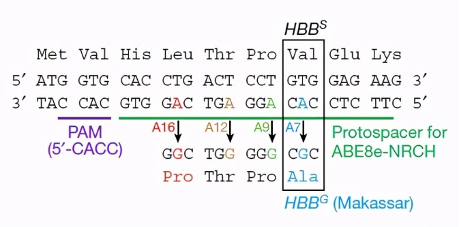
01 实验设计与小鼠模型
该疗法虽然目前因公司管线调整,暂停IND申请,但前期的临床前实验数据如下:
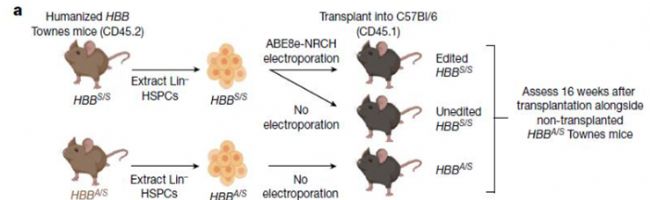
研究团队以SCD的Townes(#013071)模型开展实验,通过电穿孔的方式将修复基因导入HSPC,随后进行移植。
02 药效评估
结果表明,初次和二次移植后,这些编辑后的造血干细胞能够长期存在,并将镰状细胞病小鼠模型的血液学参数恢复到接近正常水平,SCD病理特征减轻[2]。
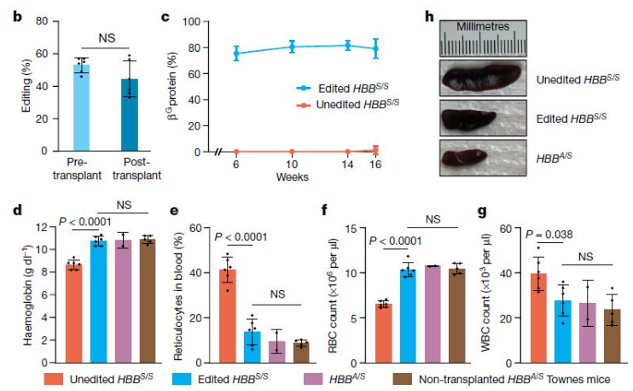
Inhibition——
CRISPR Therapeutics/Vertex: exa-cel; CTX001
CRISPR Therapeutics/Vertex: exa-cel; CTX001
除了可以添加β链外,科学家发现虽然大多数情况下,胎儿血红蛋白HbF在出生后迅速降低,但是在一些人群观察到了HbF的持续高表达,称为HPFH。如果这些人同时也携带地贫或SCD突变的话,病况会出现不同程度的减轻。
2号染色体上的BCL11A是γ链的有效抑制因子,通过抑制BCL11A将有效提高成人中HbF的含量弥补成人血红蛋白的缺失,延长疾病小鼠的寿命。像CRISPR Therapeutics/Vertex公司的CTX001,将有望成为第一个上市的CRISPR基因编辑疗法。
01 实验设计与小鼠模型
早期的临床前实验中,使用的小鼠模型如下:Bcl11a全身敲除小鼠是致死的,早期研究中通过Bcl11afl/fl和EpoR-Cre+(#035702)两种品系杂交,后再与Townes模型(#013071)杂交,达到在SCD小鼠敲除红系细胞的Bcl11a的目的[3]。
02 药效评估
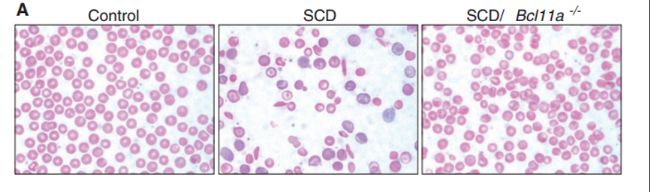
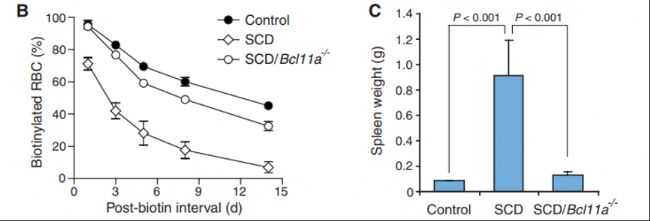
与对照相比,在红细胞Bcl11a敲除小鼠中,γ链含量显著增加,血涂片中没有可见的镰状细胞,红细胞参数以及器官组织病理特征得到显著改善。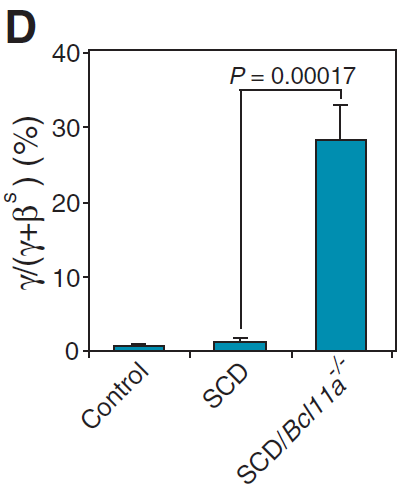
更多内容
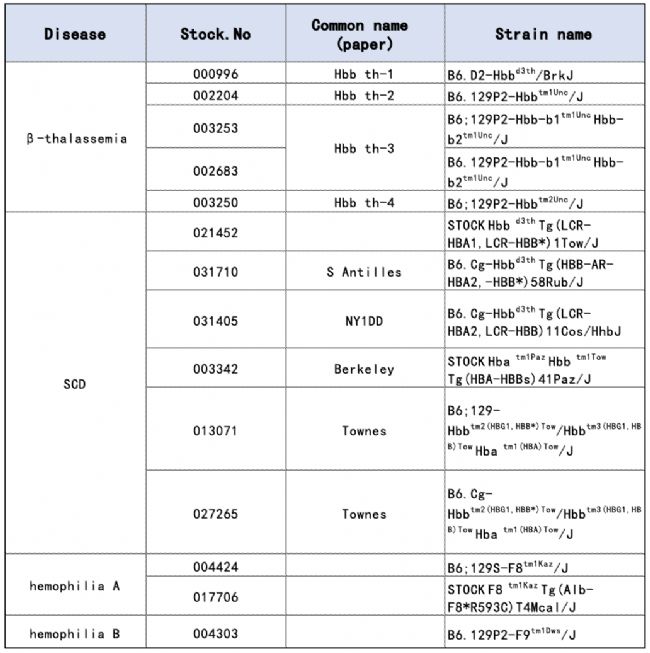
JAX常见血液类遗传疾病的小鼠模型,模型具体介绍:
☞☞三次错过好文章?你的实验还要不要做了!
参考文献:
[1] Curr Gene Ther. 2015. PMID: 25429463
[2] Nature. 2021.PMID: 34079130
[3] Science. 2011. PMID: 21998251






