Nature(IF 69.504)16S+代谢+转录揭示间歇性禁食促进神经损伤的修复

哺乳动物神经系统损伤后,神经元的再生能力因轴突再生缓慢而受到严重影响。已有研究表明,通过间歇性禁食(IF)可激活与突触再生促进相关的信号通路,包括基因转录、蛋白合成、线粒体代谢等,然而间歇性禁食是否能影响轴突的再生能力仍有待研究。
2022年6月22日,英国伦敦帝国理工学院脑科学系的Serger团队在Nature (IF 69.5042)杂志上发表题为“The gut metabolite indole-3 propionate promotes nerve regeneration and repair”的研究,通过建立小鼠坐骨损伤模型,运用非靶代谢+靶向代谢联合探究发现,间歇性禁食(IF)可引起血清中吲哚-3-丙酸(IPA)代谢物的升高,进而促进神经的再生与修复。作者同时通过16S rDNA测序及粪便移植实验证明在促神经再生时,起关键作用的微生物是革兰氏阳性菌。转录组测序和抗体实验揭示IPA可通过中性粒细胞趋化作用参与神经再生。

研究材料
小鼠背根神经节;小鼠血清
技术路线
步骤1:代谢组学分析不同饮食方式对坐骨神经损伤小鼠的影响;
步骤2:16S测序探究IPA代谢物改变的微生物因素;
步骤3:万古霉素验证微生物介导的代谢效果;
步骤4:菌株侵染和灌胃实验证明IPA影响小鼠DRG神经元生长;
步骤5:转录组测序挖掘CXCR2介导坐骨神经损伤修复;
步骤6:生理指标反应IPA促进神经支配。
研究结果
1. 表型分析: 间歇性禁食可改变坐骨神经损伤后代谢物的富集情况
建立小鼠坐骨神经挤压模型,并对损伤小鼠分别进行10天间歇性禁食(IF)和常规饮食(AL)处理,72小时可观察到IF可促进轴突再生。对两组小鼠的血清进行非靶向代谢组学,找到了14种富集程度不同代谢物,其中富集程度前四的代谢物是由微生物衍生的3-吲哚乙酸2、2,3-丁二醇2、木糖2和吲哚-3-丙酸(IPA)。提示,IF喂养后肠道微生物及代谢物变化可能对轴突再生起到关键调控。
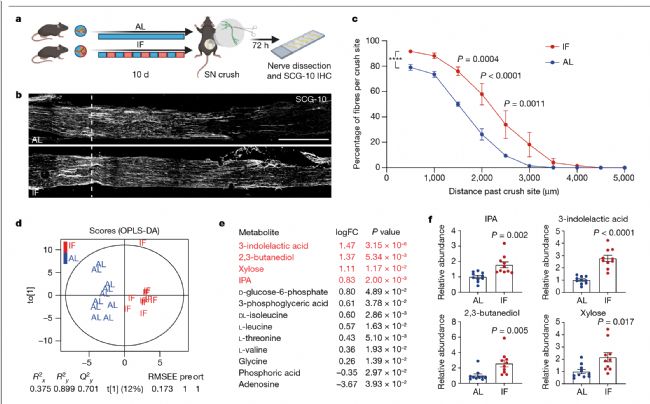
图1 IF可介导代谢物变化促进轴突再生
2. 锁定菌群:IF依赖性轴突再生需要革兰氏阳性菌
有研究表明万古霉素可用于治疗细菌感染。作者从IF组收集粪便移植到AL组,并加入万古霉素处理。通过对四组小鼠损伤及恢复后的坐骨神经分析,发现万古霉素会消除IF对轴突再生的促进作用。通过靶向代谢分析血清样本,IPA与万古霉素有最显著的相关性,且万古霉素可以抑制IPA的增加。
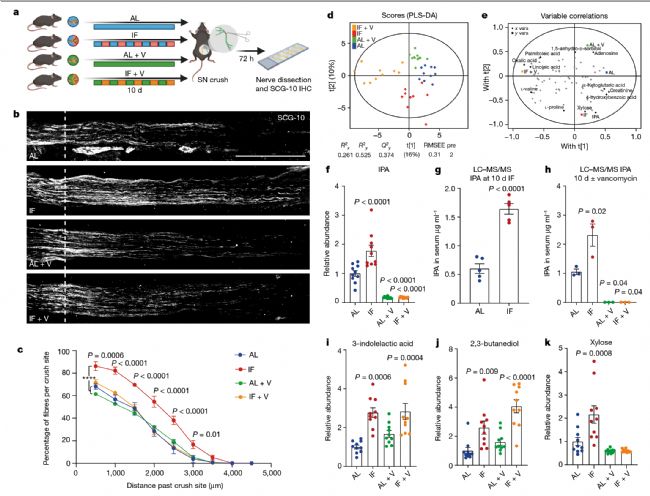
图2 IF通过肠道革兰氏阳性菌群产生IPA促进轴突再生
3. 关键功能菌群探索:万古霉素显著降低了细菌多样性
对四组小鼠盲肠进行16S rDNA扩增子测序,验证万古霉素对不同处理组中菌群的影响。结果显示万古霉素显著降低了细菌多样性,拟杆菌和厚壁菌在万古霉素的影响下丰度显著降低,在IF干预后增加。IF干预后丰度增加最多的五种细菌也属于梭状芽孢杆菌目,这证实万古霉素治疗会影响依赖性通路。
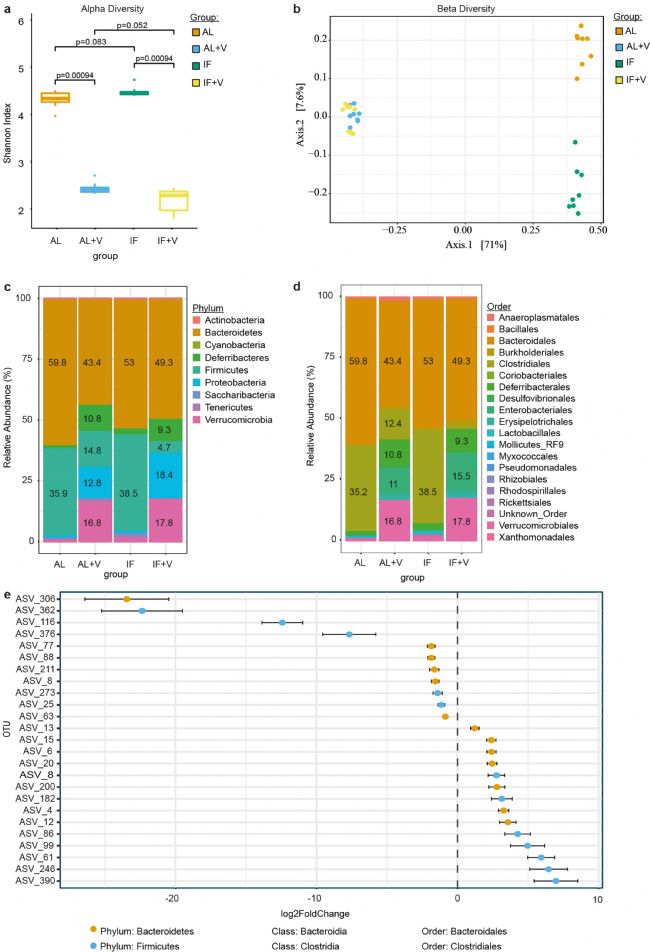
图3 万古霉素和IF会影响微生物变化
4. 菌群代谢物功能分析:IPA促进坐骨神经损伤后DRG神经元轴突再生
为研究轴突再生是否与由肠道微生物合成IPA相关,在万古霉素去除小鼠肠道内的革兰氏阳性菌后,用不能产生IPA的C.s. fldC菌株和C.s. WT菌株侵染肠道,并在坐骨神经损伤后72小时检测轴突再生情况。结果证明C.s. fldC菌株组小鼠轴突再生显著减少,且通过每日灌胃20mg kg-1 IPA可显著增加小鼠坐骨神经的轴突再生,表明血清IPA可能分别通过神经元内源性或神经元外源性机制直接或间接影响背根神经节(DRG)的神经元生长。当损伤后添加IPA时,免疫标记物SCG-10和右旋糖酐的表达分布证明了轴突再生。
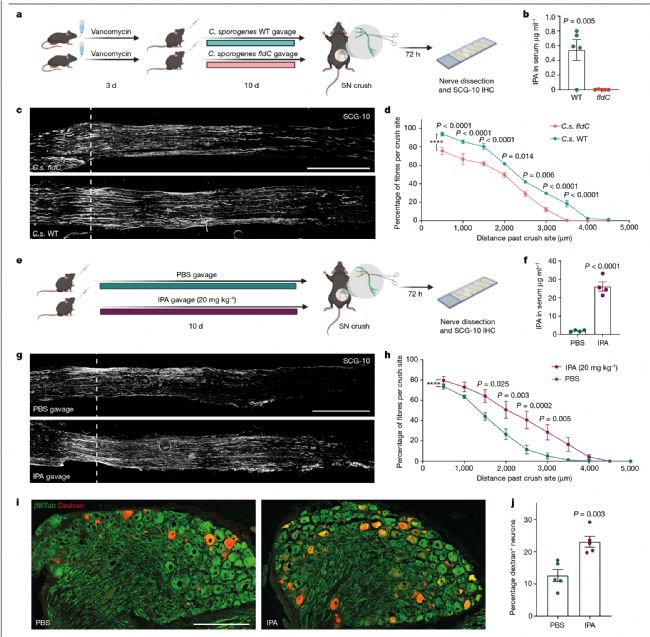
图4 IPA促进坐骨神经损伤后DRG神经元轴突再生
5. 菌群代谢物治疗效果探索:IPA治疗影响DRG基因表达程序和中性粒细胞数量
对健康小鼠DRG、接受IPA灌胃10天的小鼠坐骨神经损伤后72小时、3天两个时间点的DRG,以及对PBS口服灌胃小鼠DRG,进行RNA测序分析和抗体实验。结果证明,IPA可能通过CXCR2介导促进中性粒细胞数量变化,但这种变化仅发生在DRG区域,未发生在损伤区域。
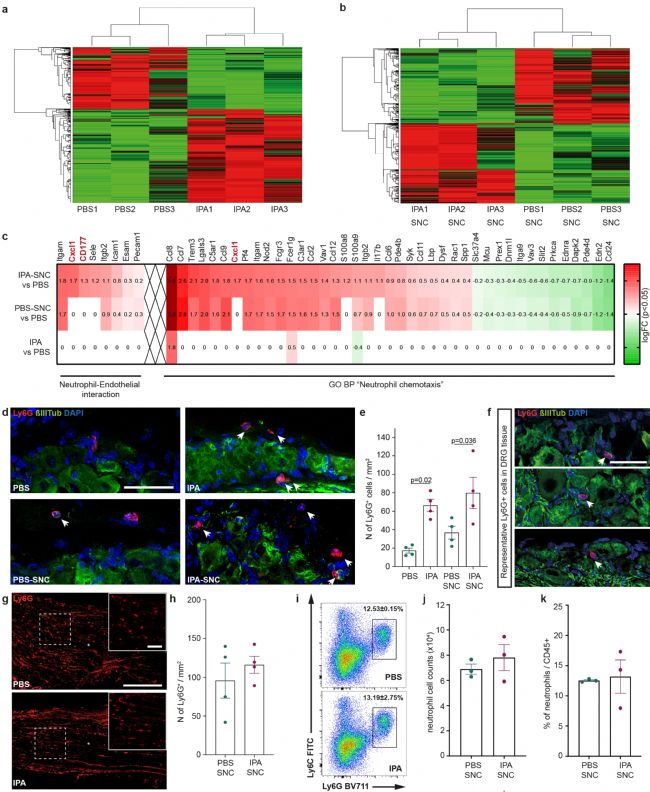
图5 IPA治疗改变DRG基因表达并增加中性粒细胞数量
6. 菌群代谢物治疗效果探索:IPA促进修复和皮肤神经支配
为了探究IPA是否可以加快损伤修复,通过热刺激反应和机械疼痛反应来评估生理感受功能的恢复。结果表明IPA处理的小鼠从热伤害中恢复得更快,即可通过改善表皮神经分布而诱导感觉恢复,但不会引起神经病理性疼痛。
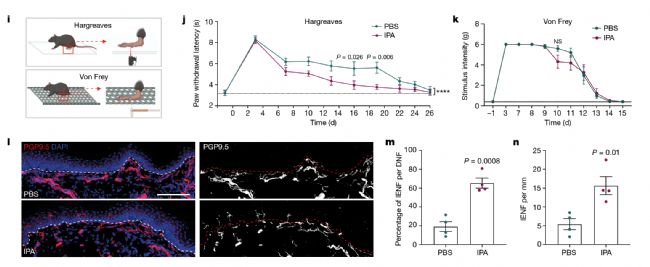
图6 IPA加快损伤修复且影响神经支配
小编小结
本研究通过建立小鼠坐骨损伤模型,采用不同饮食方法干预,并用抗生素进行干扰验证。采用代谢组学+16S+转录组测序的多组学联合模式,表明了一种依赖于间歇性禁食调控微生物菌群,进而产生IPA代谢物变化的神经再生机制。该研究为神经损伤、促进轴突再生和增强神经恢复提供新的治疗策略。





