NK细胞研发加速计划:hIL-15 NOG小鼠优惠活动开启
NK细胞在细胞疗法和抗体药物等抗肿瘤疗法中都具有极大的应用和开发优势。而在临床前体内探究中,NK细胞往往因为缺乏合适的生存环境而很快殆尽,限制实验开展。
hIL-15 NOG小鼠,在NOG背景上(超重度免疫缺陷)表达人白介素-15,进一步缩小人鼠间免疫环境的差异,支持NK细胞在体内稳定重建、扩增与功能性表达,长达8-12周之久。可应用于CAR-NK, 基于ADCC效应的抗体疗法、NKT等肿瘤免疫疗法的研发与评价。

有效性评价
抗原CD123,广泛高表达在急性髓系白血病(AML)各分化阶段的肿瘤细胞表面,与预后不良高度相关。而在正常组织(如骨髓来源造血细胞中)表达量低,是一个很有研究潜力的治疗靶点。
同种异体来源的CAR.CD123-NK可特异性靶向CD123+AML,在hIL-15 NOG小鼠进行体内的有效性及安全性验证[1]。hIL-15 NOG小鼠“超重度免疫缺陷+持续分泌人IL-15”的特点,与AML患者清淋后等待接受细胞疗法时的状态高度相似。动物进行肿瘤细胞移植后,接受CAR.CD123-NK细胞治疗: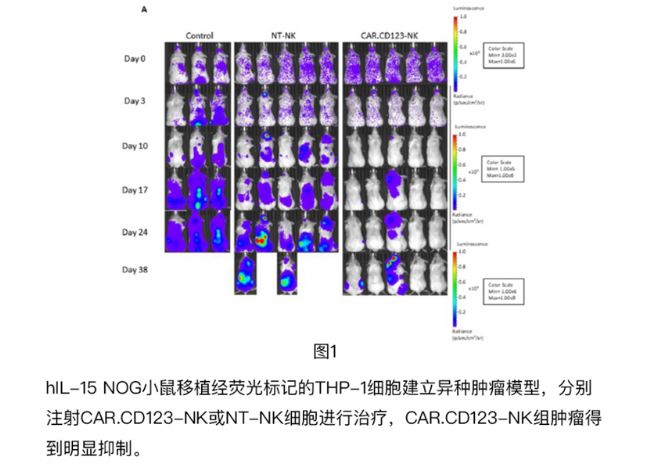

而使用传统超重度免疫缺陷模型(NSG)建立的CDX模型,虽然可观测到明显的药效,但在外周血中效应细胞存续不足14天,且未检测到相关细胞因子或毒素的释放。
安全性评价
证明CAR.CD123-NK的有效性后,研究者进一步对该细胞产品进行安全性验证。
CD123不仅存在于AML肿瘤细胞表面,在正常内皮细胞表面也存在低水平表达。有研究发现CAR.CD123-T细胞可特异性溶解CD123+内皮细胞[2]。IFN-γ和TNF-α可进一步上调内皮细胞的CD123表达量,加剧非肿瘤组织的在靶效应(On target, off tumor effect)[3]。使用hIL-15 NOG小鼠皮下接种人内皮细胞后注射CAR.CD123-NK细胞。内皮组织移植成功,其内部可见丰富的新生毛细血管网,但未见NK细胞浸润(图4),同时外周血中可检测到CAR-NK。
说明:CAR.CD123-NK在体内有效扩增的同时与正常组织的CD123特异性结合程度低,对机体的毒性弱于CAR.CD123-T,更具有安全性。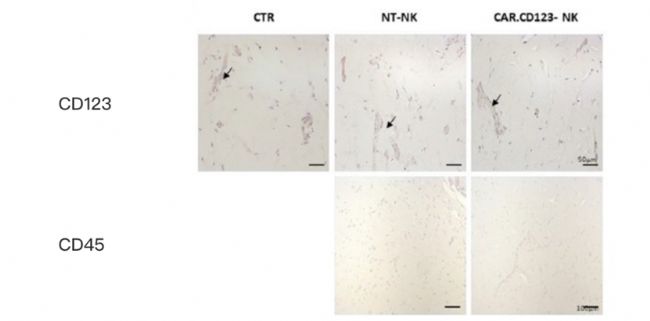
研究者同时使用huHSC-NOG-EXL小鼠验证CAR.CD123-NK对造血干细胞无潜在毒性。而CAR.CD123-T细胞则会大量杀伤外周血中的CD123+细胞,其中包括大量的正常髓系细胞(CD33+),并导致动物死亡。
用于制作细胞产品的NK细胞来源多样,除外周血、脐带血来源外,诱导多功能干细胞(iPSC)也广受青睐。因其可持续提供稳定一致的NK细胞,实现标准化生产。全球已有多个iPSC来源的NK细胞疗法在推进中。
美国Caribou 在研的iPSC-derived CAR-NK靶向ROR1+肿瘤[4]。临床前使用hIL-15 NOG小鼠作为体内药效模型,比较不同CAR结构的iNK细胞的肿瘤杀伤作用(图5)。

小结
hIL-15 NOG可进一步模拟人的免疫环境,持续分泌IL-15,为不同来源的CAR-NK细胞提供适宜扩增、存续和功能性表达的体内环境。用于CAR-NK产品临床前的有效性及安全性评价,帮助研究者进一步了解和预测CAR-NK在临床中的应用特点。

NK细胞的经典功能是通过CD16介导抗体依赖性细胞介导的细胞毒性(ADCC),杀死肿瘤细胞。抗体药物开发中,对抗体药物的Fc段进行改造可促进与CD16的结合,从而刺激或增强ADCC效应,达到更好的治疗效果。将纯化的huNK细胞移植到hIL-15 NOG小鼠体内,可用于评估抗体药物的ADCC效应。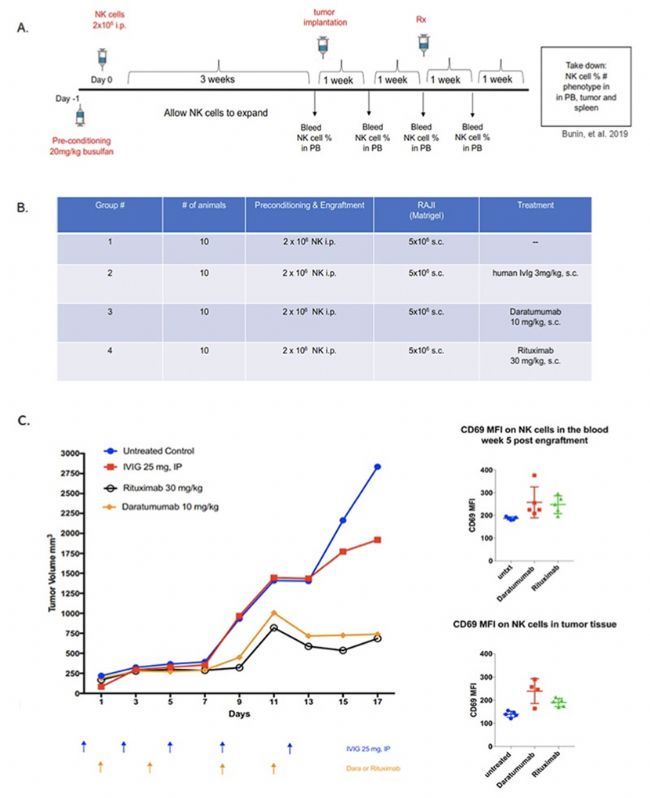

客户合作数据

除了NK细胞外,hIL-15 NOG也可用于支持与NK细胞有类似功能的免疫细胞疗法探究。NKT细胞作为T细胞的子集,可共表达NK细胞相关的标记物,在抗肿瘤免疫和肿瘤免疫监测中起着重要的作用,被应用于新型疗法的开发中。实验发现[7]:iNKT在NOG中存续不足14天,需额外补充IL-15延长细胞药物的存活时间。
使用hIL-15 NOG作为体内药效模型,可保证iNKT在体内作用时间,提高评估抗肿瘤药效的准确度,同时减少外源性输注细胞因子的工作量[8]。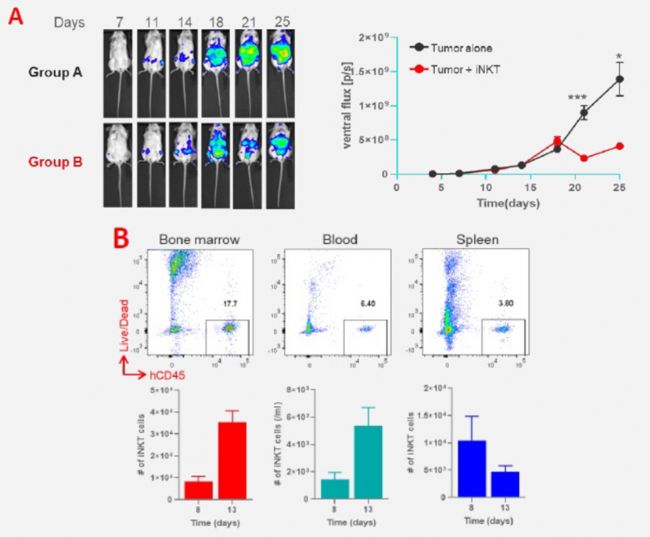
总结
hIL-15 NOG小鼠可表达IL-15,进一步模拟人体内免疫环境,支持移植NK细胞在小鼠体内稳定持续的扩增与功能性表达。维通利华也可提供huNK-hIL-15 NOG现货模型(供体已筛选),用于NK细胞相关疗法与药物的ADCC效应开发与评估。
参考文献
1. Caruso, Simona et al. “Safe and effective off-the-shelf immunotherapy based on CAR.CD123-NK cells for the treatment of acute myeloid leukaemia.” Journal of hematology & oncology vol. 15,1 163. 5 Nov. 2022, doi:10.1186/s13045-022-01376-3
2. Tettamanti, Sarah et al. “Targeting of acute myeloid leukaemia by cytokine-induced killer cells redirected with a novel CD123-specific chimeric antigen receptor.” British journal of haematology vol. 161,3 (2013): 389-401. Doi:10.1111/bjh.12282
3. Park, Jae H et al. “Long-Term Follow-up of CD19 CAR Therapy in Acute Lymphoblastic Leukemia.” The New England journal of medicine vol. 378,5 (2018): 449-459. Doi:10.1056/NEJMoa1709919
4. Rodolfo Gonzalez et al. “CB-20, an induced pluripotent stem cell (iPSC)-derived allogeneic CAR-NK cell therapy, engineered for enhanced activity against solid tumors.” 12th AACR-JCA Joint Conference, Dec. 2022, https://www.cariboubio.com/file.cfm/11/docs/cb-020_poster_aacr-jca_2022.pdf.
5. Anna Bunin, Ann Marie Rossi, Christian Vidal, David Trihn, Marco Garcia, Joseph Woska, Lawrence Iben, Luca Rastelli, Paul Volden, Enrique Alvarez; Abstract 1478: Human transgenic IL-15 NOG mice reconstituted with human NK cells as a model for NK cell depletion. Cancer Res 1 July 2019; 79 (13_Supplement): 1478. https://doi.org/10.1158/1538-7445.AM2019-1478
6. Katano, Ikumi et al. “Long-term maintenance of peripheral blood derived human NK cells in a novel human IL-15- transgenic NOG mouse.” Scientific reports vol. 7,1 17230. 8 Dec. 2017, doi:10.1038/s41598-017-17442-7
7. Yamada, Daisuke et al. “Efficient Regeneration of Human Vα24+ Invariant Natural Killer T Cells and Their Anti-Tumor Activity In Vivo.” Stem cells (Dayton, Ohio) vol. 34,12 (2016): 2852-2860. doi:10.1002/stem.2465
8. Yigit B, Moskowitz D, Michelet X, et al205 AgenT-797, a native allogeneic ‘off-the-shelf’ iNKT cell therapy product shows anti-tumor activity in preclinical xenograft modelsJournal for ImmunoTherapy of Cancer 2021;9:doi: 10.1136/jitc-2021-SITC2021.205
hIL-15 NOG小鼠,在NOG背景上(超重度免疫缺陷)表达人白介素-15,进一步缩小人鼠间免疫环境的差异,支持NK细胞在体内稳定重建、扩增与功能性表达,长达8-12周之久。可应用于CAR-NK, 基于ADCC效应的抗体疗法、NKT等肿瘤免疫疗法的研发与评价。

有效性评价
抗原CD123,广泛高表达在急性髓系白血病(AML)各分化阶段的肿瘤细胞表面,与预后不良高度相关。而在正常组织(如骨髓来源造血细胞中)表达量低,是一个很有研究潜力的治疗靶点。
同种异体来源的CAR.CD123-NK可特异性靶向CD123+AML,在hIL-15 NOG小鼠进行体内的有效性及安全性验证[1]。hIL-15 NOG小鼠“超重度免疫缺陷+持续分泌人IL-15”的特点,与AML患者清淋后等待接受细胞疗法时的状态高度相似。动物进行肿瘤细胞移植后,接受CAR.CD123-NK细胞治疗:
- 在hIL-15 NOG小鼠体内可观察到明显的抗肿瘤作用(图1),证明CAR.CD123-NK的有效性。
- NK细胞在IL-15的支持下可持续扩增,在体内持续至少30天且无毒性,CAR.CD123-NK细胞水平显著高于对照组(NT-NK)(图2)。
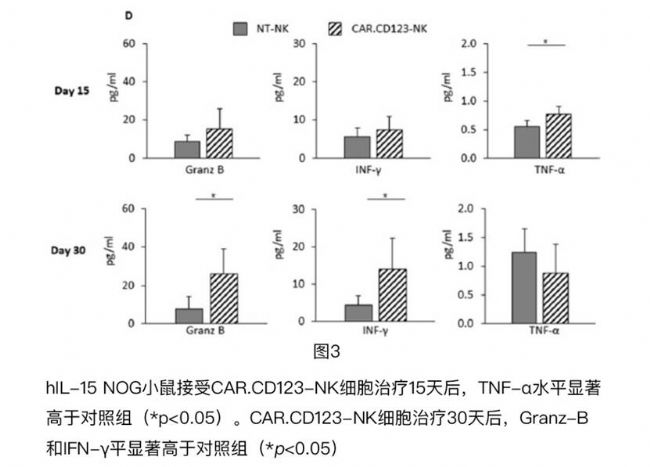
- IL-15支持扩增后的NK细胞释放出一系列细胞因子和毒素,包括TNF-α、IFN-γ和Granz-B,持续到注射后30天,为CAR.CD123-NK有效抑制肿瘤提供了数据支持(图3)。
- 根据NK细胞表面特异性标记物(CD16, CD57和PD-1)随时间的变化,研究者可进一步了解CAR.CD123-NK在体内的表型特点,并评估联合CAR-NK与发挥ADCC效应的单抗治疗的可能。



安全性评价
证明CAR.CD123-NK的有效性后,研究者进一步对该细胞产品进行安全性验证。
CD123不仅存在于AML肿瘤细胞表面,在正常内皮细胞表面也存在低水平表达。有研究发现CAR.CD123-T细胞可特异性溶解CD123+内皮细胞[2]。IFN-γ和TNF-α可进一步上调内皮细胞的CD123表达量,加剧非肿瘤组织的在靶效应(On target, off tumor effect)[3]。使用hIL-15 NOG小鼠皮下接种人内皮细胞后注射CAR.CD123-NK细胞。内皮组织移植成功,其内部可见丰富的新生毛细血管网,但未见NK细胞浸润(图4),同时外周血中可检测到CAR-NK。
说明:CAR.CD123-NK在体内有效扩增的同时与正常组织的CD123特异性结合程度低,对机体的毒性弱于CAR.CD123-T,更具有安全性。

图4:hIL-15 NOG小鼠人内皮细胞组织免疫组化染色结果。CAR.CD123-NK组中可见内皮组织重建(CD123),未见hCD45+细胞浸润(代表NK细胞)。
研究者同时使用huHSC-NOG-EXL小鼠验证CAR.CD123-NK对造血干细胞无潜在毒性。而CAR.CD123-T细胞则会大量杀伤外周血中的CD123+细胞,其中包括大量的正常髓系细胞(CD33+),并导致动物死亡。
用于制作细胞产品的NK细胞来源多样,除外周血、脐带血来源外,诱导多功能干细胞(iPSC)也广受青睐。因其可持续提供稳定一致的NK细胞,实现标准化生产。全球已有多个iPSC来源的NK细胞疗法在推进中。
美国Caribou 在研的iPSC-derived CAR-NK靶向ROR1+肿瘤[4]。临床前使用hIL-15 NOG小鼠作为体内药效模型,比较不同CAR结构的iNK细胞的肿瘤杀伤作用(图5)。

图5:hIL-15 NOG移植Jeko-1细胞后,分别接受3种不同结构的CAR-iNK细胞治疗,IVIS成像显示pCB7142 CAR-iNK缓解肿瘤符合效果最显著。
小结
hIL-15 NOG可进一步模拟人的免疫环境,持续分泌IL-15,为不同来源的CAR-NK细胞提供适宜扩增、存续和功能性表达的体内环境。用于CAR-NK产品临床前的有效性及安全性评价,帮助研究者进一步了解和预测CAR-NK在临床中的应用特点。

NK细胞的经典功能是通过CD16介导抗体依赖性细胞介导的细胞毒性(ADCC),杀死肿瘤细胞。抗体药物开发中,对抗体药物的Fc段进行改造可促进与CD16的结合,从而刺激或增强ADCC效应,达到更好的治疗效果。将纯化的huNK细胞移植到hIL-15 NOG小鼠体内,可用于评估抗体药物的ADCC效应。

图6:使用hIL-15 NOG移植纯化NK细胞后,建立肿瘤模型后,分别给予Rituximab和Daratumumab两种抗体药物评价其ADCC效应[5]。

客户合作数据

图7:纯化NK细胞移植到hIL-15 NOG体内,hCD45细胞和hCD56+NK细胞水平变化,NK细胞重建水平与供体有相关性

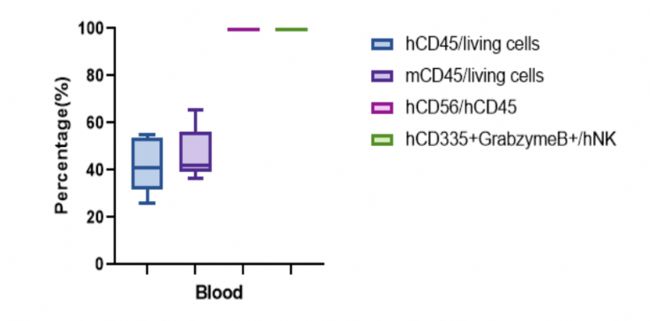
图8:huNK-hIL-15 NOG模型(B供体)移植肿瘤细胞后,外周血中各类细胞占比。

除了NK细胞外,hIL-15 NOG也可用于支持与NK细胞有类似功能的免疫细胞疗法探究。NKT细胞作为T细胞的子集,可共表达NK细胞相关的标记物,在抗肿瘤免疫和肿瘤免疫监测中起着重要的作用,被应用于新型疗法的开发中。实验发现[7]:iNKT在NOG中存续不足14天,需额外补充IL-15延长细胞药物的存活时间。
使用hIL-15 NOG作为体内药效模型,可保证iNKT在体内作用时间,提高评估抗肿瘤药效的准确度,同时减少外源性输注细胞因子的工作量[8]。

图9:在hIL-15 NOG异种肿瘤模型中,给予iNKT细胞治疗后肿瘤负荷明显减少,动物外周血、骨髓中可检测到iNKT细胞扩增
总结
hIL-15 NOG小鼠可表达IL-15,进一步模拟人体内免疫环境,支持移植NK细胞在小鼠体内稳定持续的扩增与功能性表达。维通利华也可提供huNK-hIL-15 NOG现货模型(供体已筛选),用于NK细胞相关疗法与药物的ADCC效应开发与评估。
参考文献
1. Caruso, Simona et al. “Safe and effective off-the-shelf immunotherapy based on CAR.CD123-NK cells for the treatment of acute myeloid leukaemia.” Journal of hematology & oncology vol. 15,1 163. 5 Nov. 2022, doi:10.1186/s13045-022-01376-3
2. Tettamanti, Sarah et al. “Targeting of acute myeloid leukaemia by cytokine-induced killer cells redirected with a novel CD123-specific chimeric antigen receptor.” British journal of haematology vol. 161,3 (2013): 389-401. Doi:10.1111/bjh.12282
3. Park, Jae H et al. “Long-Term Follow-up of CD19 CAR Therapy in Acute Lymphoblastic Leukemia.” The New England journal of medicine vol. 378,5 (2018): 449-459. Doi:10.1056/NEJMoa1709919
4. Rodolfo Gonzalez et al. “CB-20, an induced pluripotent stem cell (iPSC)-derived allogeneic CAR-NK cell therapy, engineered for enhanced activity against solid tumors.” 12th AACR-JCA Joint Conference, Dec. 2022, https://www.cariboubio.com/file.cfm/11/docs/cb-020_poster_aacr-jca_2022.pdf.
5. Anna Bunin, Ann Marie Rossi, Christian Vidal, David Trihn, Marco Garcia, Joseph Woska, Lawrence Iben, Luca Rastelli, Paul Volden, Enrique Alvarez; Abstract 1478: Human transgenic IL-15 NOG mice reconstituted with human NK cells as a model for NK cell depletion. Cancer Res 1 July 2019; 79 (13_Supplement): 1478. https://doi.org/10.1158/1538-7445.AM2019-1478
6. Katano, Ikumi et al. “Long-term maintenance of peripheral blood derived human NK cells in a novel human IL-15- transgenic NOG mouse.” Scientific reports vol. 7,1 17230. 8 Dec. 2017, doi:10.1038/s41598-017-17442-7
7. Yamada, Daisuke et al. “Efficient Regeneration of Human Vα24+ Invariant Natural Killer T Cells and Their Anti-Tumor Activity In Vivo.” Stem cells (Dayton, Ohio) vol. 34,12 (2016): 2852-2860. doi:10.1002/stem.2465
8. Yigit B, Moskowitz D, Michelet X, et al205 AgenT-797, a native allogeneic ‘off-the-shelf’ iNKT cell therapy product shows anti-tumor activity in preclinical xenograft modelsJournal for ImmunoTherapy of Cancer 2021;9:doi: 10.1136/jitc-2021-SITC2021.205
- 赛默飞开工福利:有奖问卷、仪器耗材促销咨询有礼
- 西安百萤生物酪胺染料限时促销,购买即免费送电影票
- 出售一批生物制药及实验室设备,包括PCR仪等
- 中乔新舟开学优惠:细胞实验套装980元,培养基折扣等
- BRAND开年大促活动来袭,移液器买就送!
- 尚恩生物开年大促销,福利叠满解锁新学期!
- 全新BTX高配置版电穿孔/电融合仪ECM 2001+特价清仓
- 助力三级细胞库建设,自动化灌装系统免费试用!
- 中乔新舟限时促销:买细胞就送支原体检测试剂盒
- 华威中仪试剂盒年末限时优惠来袭,储值享好礼
- 易科泰高光谱成像系统限时促销活动现已启动
- 美森细胞年终大促活动来袭,胎牛血清跌破底价
- Thermo NanoDrop超微量分光光度计促销正式开启
- 百萤小麦胚芽凝集素探针染料8折优惠,买即赠鼠标垫
- 真菌毒素前处理新利器―普瑞邦磁珠纯化系统特惠促销
- 南模直播预告:B细胞相关自免与炎症疾病模型的构建
- 南模今晚直播:人源化自免小鼠模型构建及其应用前景
- 李劲松院士做客南模生物直播间,讲述基因组标签计划
- 讲座:人免疫系统重建小鼠在肿瘤免疫治疗研究中应用
- 不同以“网”,智驱未来,赛业生物官网焕新升级
- 南模生物邀您相约第十六届全国免疫学学术大会
- 赛业生物品牌形象“智鼠iMouse”正式上线
- 南模生物邀您参加SAPA-China 2024医药产业大会
- 赛业生物讲座预告:Cre-loxP原理及工具鼠应用要点
- 南模生物邀您参加中国神经科学学会全国学术会议
- 赛业课程预告:基因编辑小鼠的鉴定策略及应用案例
- 南模生物邀您参加第八届全国核酸疫苗大会
- 南模生物与您相约第十七届中国实验动物科学技术年会
- 赛业将亮相ICNS2024和MDD代谢病与减肥药物开发论坛
- 南模承办生物医药浦东科技创新券资源对接交流活动